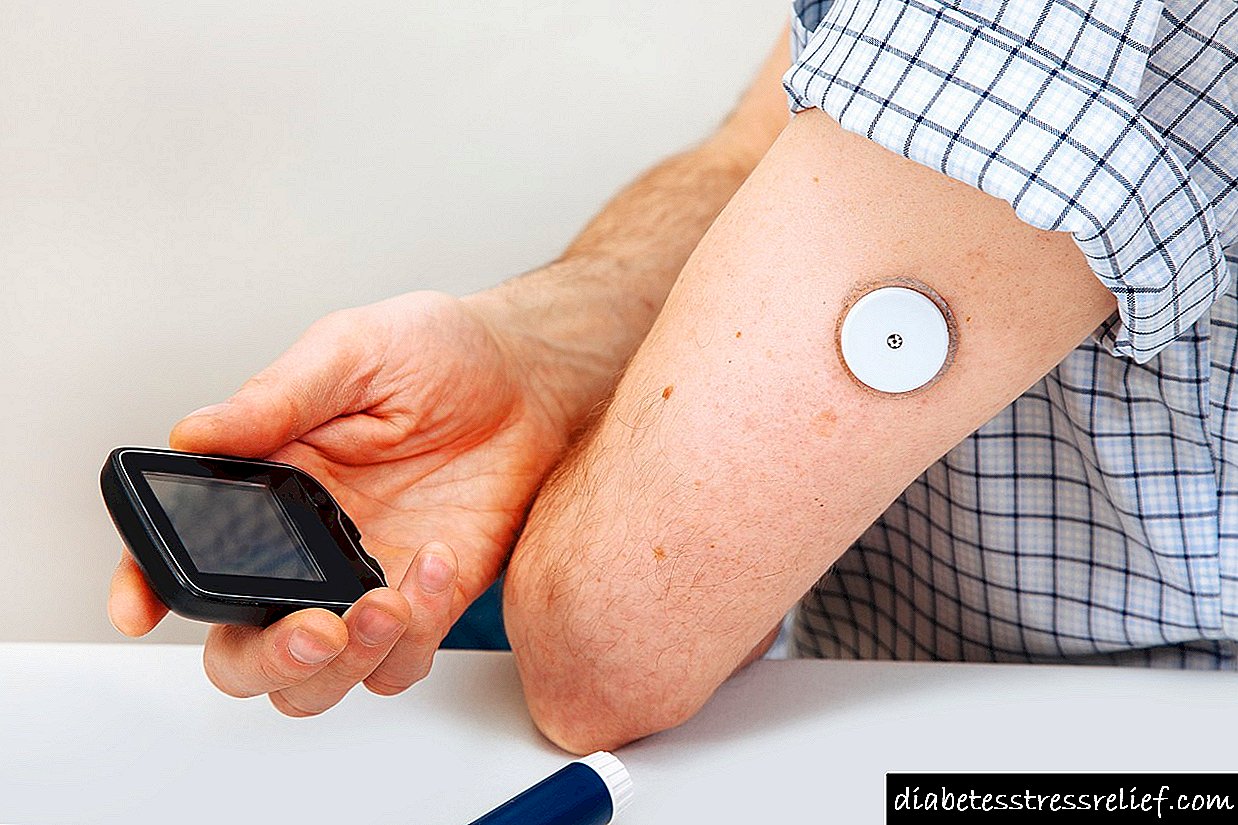
Viktoza - službena * uputstva za upotrebu
Oblik doziranja - otopina za potkožno davanje: bezbojan ili gotovo bezbojan (3 ml svaki * u staklenim ulošcima, koji se zatvoreno plastičnom olovkom za brizgalicu za jednokratnu upotrebu stavljaju u više injekcija, u kartonski svežanj od 1, 2 ili 3 olovke za štrcaljke).
* U jednoj olovci za špricu (3 ml) sadrži 10 doza od 1,8 mg, 15 doza od 1,2 mg ili 30 doza od 0,6 mg.
Aktivna supstanca: liraglutid, u 1 ml - 6 mg.
Pomoćne komponente: hlorovodonična kiselina / natrijum hidroksid q.s., natrijum hidrogen fosfat dihidrat, fenol, propilen glikol, voda za injekcije.
Farmakološka svojstva:
Farmakodinamika
Liraglutide ima dugotrajni učinak od 24 sata i poboljšava glikemijsku kontrolu snižavanjem koncentracije glukoze u krvi natašte i nakon jela kod pacijenata s dijabetesom tipa 2.
Izlučivanje inzulina ovisno o glukozi
S povećanjem koncentracije glukoze u krvi, liraglutid povećava izlučivanje inzulina. Kada se koristi postupna infuzija glukoze, izlučivanje inzulina nakon primjene jedne doze liraglutida pacijentima sa šećernom bolešću tipa 2 povećava se na razinu uporedivu s onom u zdravih ispitanika (Sl. 1).

Funkcija beta ćelije gušterače
Liraglutid je poboljšao funkciju beta ćelija gušterače, o čemu svjedoče prva i druga faza odgovora na inzulin i maksimalna sekretorna aktivnost beta ćelija. Farmakodinamička ispitivanja bolesnika sa šećernom bolešću tipa 2 pokazala su obnavljanje prve faze lučenja inzulina (intravenska primjena inzulina), poboljšanje druge faze sekrecije inzulina (hiperglikemijski test stezanja) i maksimalnu sekretornu aktivnost inzulina (test stimulacije arginina).
Tijekom terapije Viktozom ® tokom 52 tjedna došlo je do poboljšanja funkcije beta ćelija gušterače, o čemu svjedoči procjena homeostatskog modela funkcije beta stanica pankreasa (HOMA indeks) i omjera inzulina u proinzulinu.
Izlučivanje glukagona:
Liraglutid, potiče lučenje inzulina i inhibira lučenje glukagona, smanjuje koncentraciju glukoze u krvi. Liraglutid ne inhibira odgovor glukagona na niske koncentracije glukoze. Pored toga, uočena je niža proizvodnja endogene glukoze na pozadini liraglutida.
Pražnjenje želuca:
Liraglutid uzrokuje lagano kašnjenje u pražnjenju želuca, smanjujući na taj način intenzitet postprandijalne glukoze u krv.
Tjelesna težina, sastav tijela i potrošnja energije:
U ispitanika povećane tjelesne težine uključenih u dugotrajna klinička ispitivanja liraglutida, potonji je uzrokovao značajno smanjenje tjelesne težine. Skeniranje pomoću računalne tomografije (CT) i dvoenergetske rentgenske absorptiometrije (DERA) pokazalo je da je gubitak tjelesne težine nastao prvenstveno zbog gubitka pacijentovog masnog tkiva. Ovi se rezultati objašnjavaju činjenicom da se tijekom terapije liraglutidom kod pacijenata smanjuje glad i potrošnja energije.
Elektrofiziologija srca (Efc):
Učinak liraglutida na proces repolarizacije u srcu testiran je u studiji EFS-a. Primjena liraglutida u ravnotežnoj koncentraciji u dnevnoj dozi do 1,8 mg ne dovodi do produženja EPS-a.
Klinička efikasnost
3992 bolesnika sa šećernom bolešću tipa 2 randomizirano je u 5 dvostruko slijepih kliničkih ispitivanja sigurnosti i efikasnosti provedenih za procjenu učinka Victoze ® na kontrolu glikemije. Terapija Victoza ® je proizvela klinički i statistički značajno poboljšanje HbA1skoncentracije glukoze na testu i postprandijalne koncentracije glukoze u usporedbi s placebom.
Glikemijska kontrola
Lijek Viktoza ® u obliku monoterapije u trajanju od 52 tjedna izazvao je statistički značajnu vrijednost (p ®, dok je kod pacijenata koji sudjeluju u kliničkim ispitivanjima kombinirane primjene lijeka Victoza ®, prosječan HbA1s smanjen za 1,1-2,5%.
Lijek Viktoza ® tijekom 26-tjedna kombinirane terapije metforminom, preparatima sulfoniluree ili metforminom i tiazolidindionom izazvao je statistički značajne vrijednosti (p ® i metformin, dodavanje inzulina detemir osiguralo je veću učinkovitost u usporedbi s lijekom Victoza ® i metforminom nakon 26 tjedana liječenja (smanjenje HbA1c za 0,52%).
Dokazano je da je učinkovitost lijeka Victoza ® u dozi od 0,6 mg u kombinaciji sa preparatima sulfoniluree ili metformina bolja od placeba, ali je istovremeno niža nego u dozama od 1,2 mg i 1,8 mg.
Omjer pacijenata koji su postigli smanjenje HbA1s
Na osnovu monoterapije Viktozom ® tokom ispitivanja u 52 sedmici, broj pacijenata koji su postigli HbA1s ® u kombinaciji s metforminom, derivatima sulfoniluree ili kombinacijom metformina i tiazolidindiona, broj pacijenata koji su dostigli HbA1s ≤ 6,5%, statistički značajan (p ≤ 0,0001) porastao je u odnosu na broj pacijenata koji su sami primali terapiju, bez dodatka Victoze ®, hipoglikemijskim lijekovima.
U skupinama bolesnika koji nisu postigli adekvatnu kontrolu glikemije tijekom terapije Victozom ® i metforminom, postotak pacijenata koji su postigli ciljni HbA1s (® Postignut HbA1s ® kako u obliku monoterapije, tako i u kombinaciji s jednim ili dva oralna hipoglikemijska sredstva. Ovo smanjenje uočeno je već u prve dve nedelje od početka lečenja.
Postprandialna glikemija
Upotreba lijeka Victoza ® tijekom tri dana uzimanja standardne hrane pomogla je smanjenju koncentracije postprandijalne glukoze za 31-49 mg% (1,68-2,71 mmol / l).
Težina tijela
52-nedeljna monoterapija Viktozom ® bila je povezana sa stalnim gubitkom težine.
Tokom čitavog razdoblja kliničke studije, kontinuirano mršavljenje povezano je i s primjenom Victoza® u kombinaciji s metforminom i u kombinaciji s metforminom i sulfonilureom ili kombinacijom metformina i tiazolidindiona.
Gubitak tjelesne težine kod pacijenata koji su uzimali Victoza ® u kombinaciji s metforminom primijećen je i nakon dodavanja insulina detemir.
Najveće smanjenje tjelesne težine zabilježeno je kod pacijenata koji su na početku ispitivanja imali povećani indeks tjelesne mase (BMI).
Monoterapija Viktozom ® 52 tjedna uzrokovala je smanjenje prosječnog volumena struka za 3,0-3,6 cm.
Smanjenje tjelesne težine zabilježeno je kod svih bolesnika koji su primali terapiju Victozom ®, bez obzira na to jesu li ili nisu imali neželjenu reakciju u obliku mučnine.
Lijek Viktoza ® u sklopu kombinirane terapije metforminom smanjio je volumen potkožne masti za 13-17%.
Bezalkoholna steatohepatoza
Liraglutid smanjuje ozbiljnost steatohepatoze kod pacijenata sa dijabetesom tipa 2.
Krvni pritisak
Dugotrajna klinička ispitivanja pokazala su da lijek Victoza ® smanjuje sistolički krvni tlak u prosjeku za 2,3-6,7 mm Hg. u prve dve nedelje lečenja. Pad sistolnog krvnog pritiska desio se prije početka gubitka kilograma.
Ostali klinički podaci
U komparativnom istraživanju učinkovitosti i sigurnosti lijeka Victoza ® (u dozama od 1,2 mg i 1,8 mg) i inhibitora dipeptidil peptidaze-4 sitagliptina u dozi od 100 mg kod pacijenata koji nisu postigli adekvatnu kontrolu nad terapijom metforminom, najbolje smanjenje se pokazalo nakon 26 tjedana liječenja HbA1s kada se koristi lijek Victoza ® u obje doze u usporedbi sa sitagliptinom (-1.24%, -1.50% u odnosu na -0.90%, p ® u usporedbi sa sitagliptinom (43.7% i 56.0% by u usporedbi s 22,0%, p ® je bio značajno viši u usporedbi s bolesnicima koji su primali sitagliptin (-2,9 kg i -3,4 kg, u usporedbi s -1,0 kg, p ®, mučnina je bila češća. mučnina je bila prolazna, a učestalost blage hipoglikemije nije se značajno razlikovala kada su tretirane Victozom ® i sitagliptinom (0,178 i 0,161, u poređenju s 0,106 slučajeva / pacijent godišnje).1s i prednost Viktoze ® u odnosu na sitagliptin uočena je nakon 26. sedmice liječenja Viktozom ® (1,2 mg i 1,8 mg) i potvrđena je nakon 52. tjedna liječenja (-1,29% i -1,51% u usporedbi s -0.88%, p ®, što je dovelo do dodatnog i statistički značajnog smanjenja HbA1s u 78. sedmici liječenja (0,24% i 0,45%, 95 Cl: od 0,41 do 0,07 i od -0,67 do 0,23).
U komparativnoj studiji učinkovitosti i sigurnosti lijeka Victoza ® (u dozi od 1,8 mg) i exenatida (u dozi od 10 µg dva puta dnevno) kod pacijenata koji nisu postigli odgovarajuću kontrolu terapije metforminom i / ili derivatima sulfoniluree, nakon 26 tjedana upotrebe lijeka Victoza ® je uočio veće smanjenje HbA1s u usporedbi s exenatidom (-1.12% u usporedbi s -0.79%, p ® u usporedbi s exenatidom (54.2% u usporedbi s 43.4%, p = 0.0015). Obje terapije su pokazale prosječni gubitak tjelesna težina od približno 3 kg. Broj bolesnika koji su prijavili mučninu bio je niži u skupini bolesnika koji su primali lijek Viktoza ®, u usporedbi s exenatidom. Učestalost blage hipoglikemije bila je značajno manja u skupini bolesnika koji su primali lijek Viktoza ®, u usporedbi s exenatidom ( 1 932 u usporedbi s 2 600 slučajeva / pacijent godišnje, p = 0,01) Nakon 26 tjedana primjene eksenatida, pacijenti bi prebačeni su u Victoza ®, što je dovelo do dodatnog smanjenja HbA1s u 40. tjednu liječenja (-0,32%, p ® tokom 52 tjedna poboljšala je osjetljivost na inzulin u usporedbi s preparatima sulfoniluree, što je otkriveno korištenjem homeostatskog modela za procjenu otpornosti na inzulin HOMA-IR.
Farmakokinetika
Apsorpcija
Apsorpcija liraglutida nakon supkutane primjene je spora, vrijeme postizanja maksimalne koncentracije u plazmi je 8-12 sati nakon doze lijeka. Maksimalna koncentracija (C)maks) liraglutid u plazmi nakon subkutane injekcije u jednoj dozi od 0,6 mg je 9,4 nmol / L. Uvođenjem liraglutida u dozi od 1,8 mg prosječni je pokazatelj njegove ravnotežne koncentracije u plazmi (AUC?/24) dostiže približno 34 nmol / L. Izloženost liraglutida povećava se srazmjerno primijenjenoj dozi. Nakon primjene liraglutida u jednoj dozi, intrapopulacijski koeficijent varijacije na području ispod krivulje koncentracije i vremena AUC iznosi 11%. Apsolutna bioraspoloživost liraglutida nakon supkutane primjene iznosi oko 55%.
Distribucija
Prividni volumen raspodjele liraglutida u tkivima nakon potkožnog davanja je 11-17 litara. Prosječna zapremina raspodjele liraglutida nakon intravenske primjene je 0,07 l / kg. Liraglutid se veže na proteine plazme (> 98%).
Metabolizam
24 sata nakon primjene zdrave dobrovoljce jedne doze 3 H-liraglutida označenog radioaktivnim izotopom glavna komponenta plazme ostala je nepromijenjena liraglutid. Otkrivena su dva metabolita u plazmi (≤ 9% i ≤ 5% ukupne radioaktivnosti u plazmi). Liraglutid se metabolizira endogeno, poput velikih proteina, bez uključivanja bilo kojeg određenog organa kao ekskretornog puta.
Uzgoj
Nakon primjene doze od 3 H-liraglutida, nepromijenjeni liraglutid nije otkriven u urinu ili izmetu. Samo mali dio primenjene radioaktivnosti u obliku metabolita povezanih sa liraglutidom (6%, odnosno 5%) izlučivao se bubrezima ili crevima. Radioaktivne supstance izlučuju se bubrezima ili crevima, uglavnom tokom prvih 6-8 dana nakon doze leka, a sastoje se od tri metabolita. Prosječni klirens iz tijela nakon supkutane primjene liraglutida u jednoj dozi iznosi otprilike 1,2 l / h s poluvremenom eliminacije od oko 13 sati.
Posebne grupe pacijenata
Starost: Farmakokinetička ispitivanja u grupi zdravih dobrovoljaca i analiza farmakokinetičkih podataka dobivenih u populaciji bolesnika (od 18 do 80 godina) pokazuju da dob nema klinički značajan utjecaj na farmakokinetička svojstva liraglutida.
Pol: Populacijska farmakokinetička analiza podataka dobivenih proučavanjem učinka liraglutida kod žena i muškaraca te farmakokinetička ispitivanja u skupini zdravih dobrovoljaca pokazuju da spol nema klinički značajan utjecaj na farmakokinetička svojstva liraglutida.
Etnička pripadnost: Populacijska farmakokinetička analiza podataka dobivenih proučavanjem učinaka liraglutida na ispitanike rasne skupine bijele, crne, azijske i latinoameričke regije sugerira da etnička pripadnost nema klinički značajan utjecaj na farmakokinetička svojstva liraglutida.
Gojaznost: Populacijska farmakokinetička analiza podataka pokazuje da indeks tjelesne mase (BMI) nema klinički značajan utjecaj na farmakokinetička svojstva liraglutida.
Zatajenje jetre:
Farmakokinetička svojstva liraglutida proučavana su u kliničkoj studiji pojedinačne doze lijeka kod osoba s različitim stupnjem zatajenja jetre. U ispitivanje su uključeni bolesnici s blagom hepatičkom insuficijencijom (prema klasifikaciji Child Pugh-a, težina bolesti od 5 do 6 bodova) i teškom jetrenom insuficijencijom (prema klasifikaciji Child Pugh, težina bolesti> 9 bodova). Izloženost liraglutida u skupini bolesnika s oštećenom funkcijom jetre nije bila veća od one u skupini zdravih ispitanika, što ukazuje da zatajenje jetre nema klinički značajan utjecaj na farmakokinetiku liraglutida.
Zatajenje bubrega:
Farmakokinetika liraglutida proučavana je u bolesnika s različitim stupnjem bubrežne insuficijencije u jednoj studiji s jednom dozom. Ovo istraživanje je obuhvatilo ispitanice sa različitim stepenom bubrežnog zatajenja: od blage (procjena klirensa kreatinina od 50-80 ml / min) do teške (procjena klirensa kreatinina ® kod djece nije izvršena.
Podaci pretkliničke sigurnosti
Rezultati pretkliničkih toksikoloških studija uz uvođenje ponovljenih doza lijeka, uključujući genotoksičnost, pokazali su da primjena liraglutida ne predstavlja prijetnju po zdravlje ljudi.
C-ćelije štitnjače u stanicama i miševima identificirane su tijekom dvogodišnjih studija o kancerogenosti lijeka kod glodavaca i nisu dovele do smrti. U štakora nije utvrđena netoksična doza (NOAEL). Pojava takvih tumora kod majmuna liječenih liraglutidom 20 mjeseci nije primijećena. Rezultati dobiveni u studijama na glodavcima povezani su s činjenicom da su glodavci posebno osjetljivi na negetotoksični mehanizam posredovan receptorom GLP-1. Značaj podataka dobijenih za ljude je mali, ali ih nije moguće u potpunosti isključiti. Nije uočena pojava bilo kojih drugih neoplazmi povezanih s terapijom.
Studije na životinjama nisu otkrile direktan štetni učinak lijeka na plodnost, ali došlo je do blagog porasta učestalosti rane embrionalne smrti tijekom liječenja najvećom dozom lijeka. Uvođenje lijeka Viktoza ® štakorima usred njihove trudnoće uzrokovalo im je smanjenje tjelesne težine majke i rast zametaka s nepotpuno proučenim učinkom na rebra, te odstupanja u skeletnoj strukturi u skupini zečeva. Rast novorođenčadi u skupini štakora smanjio se tijekom terapije Victozom ®, a ovo smanjenje trajno se nastavilo nakon dojenja u skupini modela koji su primali velike doze liraglutida. Nije poznato što je uzrokovalo takav pad rasta novorođenih štakora - smanjenje potrošnje majke u mlijeku zbog izravnog utjecaja GLP-1, ili nedovoljna proizvodnja majčinog mlijeka od strane majke za štakore zbog smanjenog unosa njihovih kalorija.
Dozni oblik
Subkutana otopina 6 mg / ml
Sadrži 1 ml rastvora
aktivna supstanca - liraglutid 6 mg,
pomoćni sastojci: natrijum hidrogenfosfat dihidrat, propilen glikol, fenol, hlorovodonična kiselina (2M rastvor) / natrijum hidroksid (2M rastvor), voda za injekcije.
Prozirna bezbojna ili gotovo bezbojna otopina, praktično bez mehaničkih nečistoća.
Doziranje i primjena
Lijek Viktoza® primjenjuje se jednom dnevno u bilo koje vrijeme, bez obzira na unos hrane, može se primijeniti kao potkožna injekcija u trbuh, bedra ili ramena. Mjesto i vrijeme ubrizgavanja mogu varirati bez prilagođavanja doze. Međutim, poželjno je uzimati lijek otprilike u isto doba dana, u vrijeme koje je za pacijenta najpovoljnije. Daljnje informacije o načinu upotrebe lijeka Viktoza® mogu se naći u odjeljku za uporabu i zbrinjavanje. Lijek Viktoza® se ne može koristiti za intravensku i intramuskularnu primjenu.
Početna doza Victoza® iznosi 0,6 mg dnevno. Nakon upotrebe lijeka najmanje jednu sedmicu, dozu treba povećati na 1,2 mg. Postoje dokazi da se kod nekih pacijenata korist liječenja povećava s povećanjem doze lijeka s 1,2 mg na 1,8 mg. Da bi se postigla najbolja kontrola glikemije u bolesnika i uzela u obzir klinička učinkovitost, doza Viktoza® može se povećati na 1,8 mg nakon upotrebe u dozi od 1,2 mg tokom najmanje jednog tjedna. Ne preporučuje se upotreba lijeka u dnevnoj dozi iznad 1,8 mg.
Lijek Victoza® može se koristiti kao dodatak postojećoj terapiji metforminom ili kombiniranom terapijom metforminom i tiazolidindionom. Terapija metforminom u kombinaciji sa tiazolidindionom može se nastaviti u trenutnim dozama.
Victoza® se može koristiti kao dodatak tijekom postojeće terapije sulfonilurejom ili u kombiniranoj terapiji metforminom i sulfonilurejom ili bazalnim inzulinom. Kada se Viktoza® doda u sulfonilureju ili bazalnu terapiju inzulinom, potrebno je razmotriti smanjenje doze sulfonilureje ili bazalnog inzulina kako bi se smanjio rizik od neželjene hipoglikemije (vidjeti odjeljak „Posebna uputstva“).
Za podešavanje doze Victoza® nije potrebno samo nadziranje glukoze u krvi. Međutim, na početku terapije Viktoza®-om u kombinaciji s derivatima sulfoniluree ili s bazalnim inzulinom, može se zahtijevati takav samo-nadzor glukoze u krvi radi podešavanja doze preparata sulfonilureje.
Posebne grupe pacijenata
Starije osobe (> 65 godina): Nije potreban odabir doze, ovisno o dobi. Postoji ograničeno iskustvo s primjenom lijeka kod pacijenata starih 75 godina i više (vidjeti dio „Farmakokinetika“).
Pacijenti sa oštećenom funkcijom bubrega
Nema potrebe za prilagodbom doze u liječenju bolesnika s blagim oblikom bubrežnog zatajenja (klirens kreatinina 60 - 90 ml / min). Postoji samo vrlo ograničeno iskustvo u liječenju pacijenata s umjerenom bubrežnom insuficijencijom (klirens kreatinina 30–59 ml / min) i nema podataka o liječenju bolesnika s teškim zatajenjem bubrega (klirens kreatinina ispod 30 ml / min). Trenutno se Victoza ne preporučuje za upotrebu pacijentima s teškim ili umjerenim oblicima bubrežnog zatajenja, uključujući bolesnike u terminalnom stadijumu bubrežne bolesti (vidjeti odjeljak Farmakokinetika)
Pacijenti s oštećenom funkcijom jetre
Iskustvo liječenja pacijenata sa svim oblicima zatajenja jetre (blago, umjereno i teško) trenutno je previše ograničeno da bi preporučilo uporabu Victoze (vidjeti odjeljak Farmakokinetika).
Pedijatrijska populacija bolesnika
Lijek Victoza ne preporučuje se djeci i adolescentima mlađim od 18 godina zbog nedostatka podataka o sigurnosti i efikasnosti njegove upotrebe.
Nuspojave
U kliničkim ispitivanjima najčešće se javljaju nuspojave iz gastrointestinalnog trakta: mučnina i proliv (zabilježeni u> 10% bolesnika), povraćanje, zatvor, bol u trbuhu i dispeptički simptomi (zabilježeni u ≥ 1%, ali ≤ 10 % pacijenata).
Na početku terapije Viktozom®, ove se gastrointestinalne nuspojave mogu pojaviti češće, ali kako se liječenje nastavlja, reakcije se obično smanjuju tijekom nekoliko dana ili tjedana. Neželjene reakcije u obliku glavobolje i infekcija gornjih disajnih puteva uočene su relativno često (1 - 10% bolesnika). Pored toga, moguć je razvoj hipoglikemijskih stanja, posebno ako se koristi lijek Victoza® u kombinaciji s derivatima sulfoniluree (registriran u> 10% bolesnika). Teška hipoglikemija uglavnom se razvija na pozadini kombinirane primjene lijeka Viktoza® sa sulfonilureama.
O ozbiljnim nuspojavama prijavljivane su vrlo rijetko.
Opis pojedinačnih nuspojava
U kliničkoj studiji koja je koristila liraglutid kao monoterapiju, incidencija hipoglikemije liraglutidom bila je niža od incidencije hipoglikemije u bolesnika liječenih referentnim lijekom (glimepirid). Najčešće neželjene reakcije uključuju gastrointestinalne bolesti, infekcije i infestacije.
Većina epizoda potvrđene hipoglikemije u kliničkim ispitivanjima bila je zanemarljiva. U studiji koja je koristila liraglutid kao monoterapiju nije bilo ozbiljnih slučajeva hipoglikemije. Ozbiljne epizode hipoglikemije nisu česte i u početku su primećene uz upotrebu liraglutida u kombinaciji sa sulfonilurejom (0,02 epizode po bolesniku u godinama). Zapažen je vrlo mali broj epizoda (0,001 epizoda po pacijentu godinama) uz primjenu liraglutida u kombinaciji sa oralnim antidijabetičkim lijekovima osim sulfoniluree. Rizik od hipoglikemije je nizak ako se kombinira primjena bazalnog inzulina i liraglutida (1,0 epizoda po bolesniku u godinama, vidjeti dio farmakodinamike).
Gastrointestinalne neželjene reakcije
Kada su se liraglutid i metformin kombinovali, 20,7% pacijenata prijavilo je barem jednu epizodu mučnine, a 12,6% pacijenata najmanje jednu epizodu proliva.
Kada se liraglutid kombinirao sa sulfonilurejom, 9,1% bolesnika prijavilo je barem jednu epizodu mučnine, a 7,9% bolesnika barem jednu epizodu proljeva. Većina nuspojava bila je blage ili umjerene prirode i imala prirodu ovisnu o dozi.
S produljenim liječenjem učestalost i težina smanjili su se kod većine pacijenata koji su u početnoj fazi imali mučninu.
U bolesnika starijih od 70 godina pri liječenju liraglutidom češće se mogu javiti gastrointestinalni poremećaji.
U bolesnika sa blagim do umerenim zatajivanjem bubrega (klirens kreatinina od 60–90 ml / min i 30–59 ml / min, respektivno) mogu se javiti više gastrointestinalnih nuspojava tokom lečenja liraglutidom.
Isključenje pacijenata iz ispitivanja
U dugoročno kontroliranim ispitivanjima (26 tjedana ili više) udio bolesnika izuzetih iz testa zbog nuspojava bio je 7,8% za bolesnike koji su bili podvrgnuti liječenju liraglutidom i 3,4% za bolesnike iz usporedne skupine liječenja. Najčešće neželjene reakcije koje su dovele do povlačenja ispitivanja u liječenju bolesnika s liraglutidom uključuju mučninu (2,8% pacijenata) i povraćanje (1,5% bolesnika).
Reakcije na mjestu ubrizgavanja
Reakcija na mjestu ubrizgavanja lijeka zabilježena je u približno 2% bolesnika tijekom dugotrajno kontroliranih kliničkih ispitivanja Victoze (26 tjedana ili više). Te su reakcije obično bile neznatne.
Tokom dugotrajnih kontroliranih kliničkih ispitivanja Victoze (26 tjedana ili više), zabilježeni su slučajevi akutnog pankreatitisa (
Kontraindikacije
- Preosjetljivost na aktivnu tvar ili drugo
komponente koje čine lijek
- upotreba kod pacijenata sa dijabetesom tipa 1
- za lečenje dijabetičke ketoacidoze
ozbiljno zatajenje bubrega i jetre
- dječja i tinejdžerska dob do 18 godina
- trudnoća i dojenje
Interakcije lijekova
Procjena interakcije lijeka in vitro
Liraglutid je pokazao nisku sposobnost farmakokinetičke interakcije lijekova zbog metabolizma u sistemu citokroma P-450 (CYP), kao i vezanja na proteine u plazmi.
Procjena interakcije lijekova in vivo
Lagano odlaganje pražnjenja želuca prilikom primjene liraglutida može utjecati na apsorpciju istodobnih lijekova namijenjenih oralnoj primjeni. Studije interakcije lijekova nisu pokazale nikakvo klinički značajno usporavanje apsorpcije ovih lijekova. Nekoliko pacijenata liječenih Victozom® imalo je najmanje jednu epizodu akutne dijareje. Proliv može utjecati na apsorpciju oralnih lijekova koji se koriste istovremeno s Victoza®.
Varfarin i drugi derivati kumarina
Studije o interakciji ova dva lijeka nisu provedene. Na početku liječenja lijekom Victoza® u bolesnika koji primaju varfarin ili druge derivate kumarina, preporučuje se češće nadziranje INR-a (međunarodnog normaliziranog odnosa).
Liraglutid nije izazvao promjenu općeg djelovanja paracetamola nakon njegove primjene u jednoj dozi od 1000 mg. Maksimalna koncentracija paracetamola u plazmi (Cmax) smanjena je za 31%, a prosječno vrijeme postizanja vrhunca njegove koncentracije (tmax) u krvnoj plazmi produženo je za 15 minuta. Uz istodobnu primjenu liraglutida i paracetamola, nije potrebno prilagođavanje doze lijeka.
Liraglutid nije uzrokovao klinički značajnu promjenu općeg učinka atorvastatina nakon njegove primjene u jednoj dozi od 40 mg. Stoga prilagodba doze atorvastatina tijekom uzimanja Victoza® nije potrebna. Maksimalna koncentracija atorvastatina u plazmi (Cmax) smanjena je za 38%, a prosječno vrijeme postizanja vrhunca koncentracije u plazmi (tmax) kod pacijenata koji su primali liraglutid produžio se za jedan do tri sata.
Liraglutid nije uzrokovao promjenu općeg učinka griseofulvina nakon njegove primjene u jednoj dozi od 500 mg. Maksimalna koncentracija griseofulvina (Cmax) porasla je za 37%, dok se prosječno vrijeme postizanja svoje vršne koncentracije (tmax) u plazmi nije promijenilo. Nije potrebno prilagođavanje doze grizeofulvina i drugih lijekova s niskom rastvorljivošću i velikom propusnošću.
Uvođenje digoksina u jednoj dozi od 1 mg uz uporabu liraglutida pokazalo je smanjenje površine ispod krivulje (AUC) digoksina za 16%, a maksimalna koncentracija digoksina u plazmi (Cmax) smanjena je za 31%. Prosječno vrijeme postizanja vršne koncentracije (tmax) digoksina tijekom uzimanja liraglutida poraslo je s jednog na sat i pol. Na temelju dobivenih rezultata prilagodba doze digoksina tijekom uzimanja liraglutida nije potrebna.
Primjena lizinoprila u jednoj dozi od 20 mg tijekom primjene liraglutida pokazala je smanjenje površine ispod krivulje (AUC) lizinoprila za 15%, a maksimalna koncentracija lizinoprila u plazmi smanjena je za 27%. Prosječno vrijeme postizanja vršne koncentracije (tmax) lizinoprila u plazmi tijekom uzimanja liraglutida povećalo se sa šest na osam sati. Na osnovu rezultata, prilagođavanje doze lizinoprila i digoksina tijekom uzimanja liraglutida nije potrebno.
Maksimalna plazma koncentracija (Cmax) etiniil estradiola i levonorgestrela u pojedinačnim dozama tijekom terapije liraglutidom smanjena je za 12%, odnosno 13%. Pod istim uvjetima prosječno vrijeme postizanja vršne koncentracije (tmax) ovih lijekova bilo je 1,5 sata kasnije nego što je to uobičajeno. Klinički značajan uticaj na ukupni efekat etinil estradiola i levonorgestrela u organizmu nema liraglutid. Dakle, očekivani kontracepcijski učinak oba lijeka tijekom terapije liraglutidom se ne mijenja.
Nisu otkrivene farmakokinetičke ili farmakodinamičke interakcije liraglutida s inzulinom detemir jednokratnom primjenom inzulina detemir u dozi od 0,5 U / kg s liraglutidom u dozi od 1,8 mg u bolesnika sa šećernom bolešću tipa 2.
Supstance dodane Victoza® mogu izazvati razgradnju liraglutida. Budući da testovi kompatibilnosti nisu provedeni, Viktoza® se ne može miješati sa drugim lijekovima, uključujući otopine za infuziju.
Posebna uputstva
Victoza® se ne smije primjenjivati u bolesnika sa šećernom bolešću tipa 1 ili za liječenje dijabetičke ketoacidoze.
Victoza® ne zamjenjuje inzulin.
Iskustvo s primjenom Victoza® u bolesnika sa srčanom insuficijencijom I-II funkcionalne klase u skladu s Funkcionalnom klasifikacijom hronične srčane insuficijencije (New York Cardiology Association - NYHA) New York Cardiology Association (NYHA) je ograničeno i stoga liraglutid treba koristiti s oprezom. Nema iskustva u liječenju bolesnika s kongestivnim zatajenjem srca III - IV klase prema klasifikaciji NYHA i stoga se imenovanje liraglutida kod takvih bolesnika ne preporučuje.
Podaci o upotrebi lijeka Viktoza® u bolesnika s upalnom bolesti crijeva i dijabetičkom parezom želuca su ograničeni, uporaba lijeka Viktoza® u ovim skupinama bolesnika nije preporučljiva. Upotreba lijeka Viktoza® povezana je s razvojem kratkoročnih nuspojava iz gastrointestinalnog trakta, kao što su mučnina, povraćanje i proljev.
Upotreba drugih agonista GLP-1 povezana je s rizikom od razvoja pankreatitisa. Zabilježeno je nekoliko slučajeva akutnog pankreatitisa. Bolesnike treba obavijestiti o karakterističnim simptomima razvoja akutnog pankreatitisa: uporni jaki bolovi u trbuhu. Ako se sumnja na pankreatitis, terapiju Victoza® i drugim potencijalno opasnim lijekovima treba odmah prekinuti.
Kada je potvrđena dijagnoza akutnog pankreatitisa, primjena lijeka Viktoza® ne bi trebala biti nastavljena. Treba biti oprezan prilikom propisivanja lijeka pacijentima koji imaju povijest pankreatitisa.
Bolest štitne žlijezde
Tijekom kliničkih ispitivanja lijeka Victoza®, prijavljene su nuspojave štitnjače, uključujući povišeni serumski kalcitonin, difuzni tirotoksični gušter i neoplazme štitnjače, pa se liraglutid treba primjenjivati s oprezom, posebno u bolesnika s postojećim bolestima štitna žlijezda (vidjeti dio „Nuspojave“).
Pacijenti koji uzimaju liraglutid u kombinaciji sa sulfonilurejom ili bazalnim insulinom mogu imati povećan rizik od hipoglikemije (vidjeti odeljak „Nuspojave“). Rizik od hipoglikemije može se smanjiti smanjenjem doze sulfonilureje ili bazalnog inzulina.
Znakovi i simptomi dehidracije, uključujući oslabljenu funkciju bubrega i akutno zatajenje bubrega, opisani su kod pacijenata koji uzimaju liraglutid. Pacijente koji uzimaju liraglutid treba upozoriti na mogući rizik od dehidracije ovisno o nuspojavama iz gastrointestinalnog trakta i preporučiti ih da preduzmu mjere opreza kako bi se spriječilo iscrpljivanje tekućine u tijelu.
Podaci pretkliničke sigurnosti
Rezultati pretkliničkih studija zasnovanih na općenito prihvaćenim istraživanjima farmakološke sigurnosti, toksičnosti uz ponovljene doze lijeka i genotoksičnosti, pokazali su da primjena liraglutida ne predstavlja prijetnju po zdravlje ljudi.
Neoplazme C-ćelija štitne žlijezde štakora i miševi otkrivene su tokom dvogodišnjeg ispitivanja onkogenosti lijeka kod glodavaca i nisu dovele do smrti. Nisu primijećeni dokazi o štetnim nuspojavama (NOAEL) kod pacova. Pojava takvih neoplazmi kod majmuna koji su 20 mjeseci liječeni liraglutidom nije primijećena. Rezultati dobiveni testovima na glodavcima povezani su s činjenicom da su glodavci posebno osjetljivi na peptid sličan glukagonu-peptidu -1 (GLP-1) ne-genotoksičnog specifičnog mehanizma. Značaj podataka dobijenih za ljude je nizak, ali ih nije moguće u potpunosti isključiti. Nije uočena pojava bilo kojih drugih neoplazmi povezanih s terapijom.
U studijama na životinjama nije bilo izravnog štetnog utjecaja lijeka na plodnost, ali došlo je do blagog porasta učestalosti rane embrionalne smrti tijekom liječenja najvećom dozom lijeka. Uvođenje lijeka Viktoza štakorima usred gestacijskog razdoblja uzrokovalo je njihovo smanjivanje tjelesne težine majke i rast embrija s učinkom na rebra koji nije u potpunosti shvaćen, te odstupanja u skeletnoj strukturi u skupini zečeva. Rast novorođenčadi u skupini štakora tijekom terapije Victozom smanjio se, a taj pad uporno je ostao i nakon razdoblja dojenja u skupini modela koji su primali velike doze liraglutida. Nije poznato što je uzrokovalo takav pad porasta novorođenih štakora - smanjenje njihove potrošnje majčinog mlijeka zbog izravnog utjecaja peptida sličnog glukagonu GLP-1, ili nedovoljne proizvodnje majčinog mlijeka od strane majke pacova zbog smanjenog unosa kalorija.
Nakon intraarterijske injekcije liraglutida kod kunića, primijećeno je blago do umjereno krvarenje, crvenilo i oticanje na mjestu uboda.
Koristite tokom trudnoće i tokom dojenja
Studije na životinjama nisu otkrile direktan štetni učinak lijeka na plodnost, ali došlo je do blagog porasta učestalosti rane embrionalne smrti tijekom liječenja najvećom dozom lijeka. Primjena Viktoza® štakorima usred njihove trudnoće uzrokovala je smanjenje tjelesne težine majke i rast zametaka s nepotpuno proučenim učinkom na rebra, te odstupanja u strukturi skeleta u grupi zečeva. Rast novorođenih jedinki u skupini štakora tijekom terapije Victozom® smanjio se, a taj pad trajno je nastavljen nakon dojenja u skupini osoba koje su primale visoke doze liraglutida. Nije poznato što je uzrokovalo takav pad rasta novorođenih štakora - smanjenje potrošnje majke u mlijeku zbog izravnog utjecaja GLP-1, ili nedovoljne razine proizvodnje majčinog mlijeka od strane majke pacova zbog smanjenog unosa njihovih kalorija.
Nisu dostupni odgovarajući podaci o upotrebi lijeka Victoza® u trudnica. Potencijalni rizik za ljude nije poznat.
Lijek Viktoza® se ne može koristiti tijekom trudnoće, već se preporučuje provođenje liječenja inzulinom. Ako se pacijentica priprema za trudnoću, ili je trudnoća već započela, terapiju Victoza®-om treba odmah prekinuti.
Nema iskustva s primjenom lijeka Victoza® u dojilja, primjena lijeka tijekom dojenja je kontraindicirana.
Značajke djelovanja lijeka na sposobnost upravljanja vozilima i potencijalno opasne mehanizme
Ispitivanje utjecaja lijeka Victoza® na sposobnost upravljanja vozilima i rada sa mehanizmima nije provedeno. Pacijente treba upozoriti da trebaju poduzeti mjere opreza kako bi se izbjegao razvoj hipoglikemije tijekom vožnje i rada s mehanizmima, posebno ako se Victoza® uzima u sklopu kombinirane terapije sulfonilureama ili s baznim inzulinom.
Predoziranje
Simptomi: tijekom kliničkog ispitivanja Victoza®, jedan od pacijenata s dijabetesom tipa 2 pretrpio je predoziranje lijeka u obliku potkožne injekcije u dozi od 72 mg (40 puta najveće preporučene doze od 1,8 mg). Predoziranje je uzrokovalo jaku mučninu i povraćanje. Nije zabilježena hipoglikemija. Pacijent se potpuno oporavio bez komplikacija.
Liječenje: preporučuje se odgovarajuća simptomatska terapija, ovisno o kliničkim znacima i simptomima.
Farmakodinamika
Liraglutid je analog ljudskog GLP-1 (glukagonu sličan peptid-1). Proizveden biotehnološkom metodom rekombinantne DNK (deoksiribonukleinska kiselina) upotrebom soja Saccharomyces cerevisiae, koji ima 97% homolognost s ljudskim GLP-1, veže i aktivira GLP-1 receptore kod ljudi.
GLP-1 receptor je meta za nativni GLP-1, koji je endogeni hormon inkretin, koji stimulira lučenje glukoze ovisno o β-ćelijama pankreasa. U usporedbi s matičnim GLP-1, farmakodinamički i farmakokinetički profili liraglutida omogućuju mu davanje jednom dnevno.
Pomoću potkožne injekcije, supstanca dugog djelovanja temelji se na tri mehanizma:
- samo-povezivanje, što omogućava odloženu apsorpciju liraglutida,
- vezivanje za albumin,
- viši nivo enzimske stabilnosti protiv DPP-4 (dipeptidil peptidaza-4) i NEP (enzim neutralna endopeptidaza), što osigurava dugo T1/2 (poluživot) tvari iz plazme.
Učinak liraglutida zasnovan je na interakciji sa specifičnim GLP-1 receptorima, uslijed čega se razina cAMP (ciklički adenozin monofosfat) povećava. Pod djelovanjem tvari opaža se stimulacija izlučivanja inzulina ovisna o glukozi i poboljšava se β-stanica pankreasa. Istovremeno, dolazi do suzbijanja glukoze pretjerano povećanog lučenja glukagona. Tako se s povećanjem koncentracije glukoze u krvi potiskuje lučenje glukagona i potiče lučenje inzulina.
S druge strane, u bolesnika sa hipoglikemijom liraglutid smanjuje lučenje inzulina bez inhibicije lučenja glukagona. Mehanizam za smanjenje glikemije uključuje i malo odlaganje pražnjenja želuca. Koristeći mehanizme koji uzrokuju smanjenje gladi i smanjenje potrošnje energije, liraglutid dovodi do smanjenja masnog tkiva i do gubitka težine.
GLP-1 je fiziološki regulator apetita i unosa kalorija, receptori ovog peptida nalaze se u nekoliko područja mozga koja su uključena u regulaciju apetita.
Tijekom provođenja ispitivanja na životinjama, ustanovljeno je da liraglutid pomoću specifične aktivacije receptora GLP-1 pojačava signale zasićenja i slabi signale gladi, što dovodi do gubitka kilograma.
Takođe, prema studijama na životinjama, liraglutid usporava razvoj dijabetesa. Supstanca je moćan faktor specifične stimulacije proliferacije β-ćelija gušterače i sprječava smrt β-ćelija (apoptoza), koju induciraju citokini i slobodne masne kiseline. Dakle, liraglutid povećava biosintezu inzulina i povećava β-staničnu masu. Nakon normalizacije koncentracije glukoze, liraglutid prestaje povećavati masu pankreasnih β-ćelija.
Victose ima dugačak 24-satni učinak i poboljšava glikemijsku kontrolu, što se postiže smanjenjem koncentracije glukoze u krvi na brzinu i nakon jela sa dijabetesom tipa 2.
Farmakološka grupa
Ostali hipoglikemijski lijekovi, osim inzulina.
Šifra ATC A10V X07.
Victoza® se koristi za liječenje dijabetesa melitusa tipa II kod odraslih kako bi se postigla kontrola glikemije u kombinaciji sa:
- metformin ili sulfonilurea kod pacijenata sa lošom kontrolom glikemije, uprkos korištenju maksimalno tolerisanih doza metformina ili sulfonilureje kao monoterapiji,
- metformin i sulfonilureje, ili metformin i tiazolidindioni kod pacijenata sa lošom kontrolom glikemije i pored dvostruke terapije.
Kombinovana terapija bazalnim inzulinom kod pacijenata koji nisu postigli dobru kontrolu glikemije uz pomoć Viktoze i metformina.
Neželjene reakcije
U pet velikih, dugotrajnih kliničkih ispitivanja, više od 2500 pacijenata dobivalo je sam Victoza® ili njegovu kombinaciju s metforminom, s glimepiridom (sa ili bez metformina), sulfonilurejom (sa ili bez metformina) ili s metforminom + rosiglitazonom.
Procjena učestalosti nuspojava provedena je na sljedećoj skali: vrlo često
(≥ 1/10), često (od ≥ 1/100 do ® - 2501). Predstavljene su slijedeće nuspojave, čija je učestalost u skupini bolesnika koji su primali lijek Viktoza® premašila za više od 5% učestalost u skupini u kojoj su primali uporedni lijek. Uključene su i neželjene reakcije, čija učestalost iznosi -1, ali javljaju se više od 2 puta češće u usporedbi s lijekom za usporedbu.
Metabolički i nutritivni poremećaji: često - hipoglikemija, anoreksija, rijetko smanjen apetit - dehidracija *.
Poremećaji nervnog sistema: često - glavobolja, vrtoglavica.
Probavni poremećaji: vrlo često - mučnina, proliv, često - povraćanje, dispepsija, bol u gornjem dijelu trbuha, zatvor, gastritis, nadimanje, nadimanje, gastroezofagealni refluks, belching, zubobolja, virusni gastroenteritis vrlo retko - (pankreatitis (uključujući nekrotični pankreatitis).
Kardiovaskularni poremećaji: često - povećani rad srca (HR).
Poremećaji imunog sistema: rijetko anafilaktičke reakcije.
Infekcije i infestacije: često - infekcije gornjih disajnih puteva (nazofaringitis, bronhitis).
Opći poremećaji i stanje na mestu ubrizgavanja: rijetko - slabost, često - umor, vrućica, reakcije na mjestu ubrizgavanja.
Poremećaji bubrega i mokraćnih puteva : rijetko - akutno zatajenje bubrega *, oslabljena bubrežna funkcija *.
Na delu kože i potkožnog tkiva : često - osip, rijetko - urtikarija, svrbež.
(* Pogledajte odjeljak Funkcije aplikacije).
Opis pojedinačnih nuspojava
Tijekom kliničkog ispitivanja monoterapije monoterapijom Viktoza®, učestalost hipoglikemije u bolesnika koji su uzimali Victoza® bila je manja nego u bolesnika koji su primali aktivni referentni lijek (glimepirid). Najčešće nuspojave bile su probavne smetnje, infekcije i infestacije.
U većini slučajeva zabilježenih tijekom kliničkih ispitivanja potvrđena hipoglikemija je zanemariva. Tijekom monoterapije Viktozom® nije zabilježen niti jedan slučaj teške hipoglikemije. Teška hipoglikemija javlja se rijetko i uglavnom se opaža kombiniranim liječenjem Viktozom® i sulfonilurejom (0,02 slučaja / godina pacijenta). Vrlo rijetko (0,001 slučaja / godina pacijenta) bilo je slučajeva hipoglikemije tijekom liječenja lijekom Victoza® u kombinaciji s drugim oralnim antidijabetičkim lijekovima (tj. Sa sulfonilurejom).
Nakon dodatne primjene inzulina pacijentima koji su uzimali detemir, primili su liraglutid 1,8 mg metformina; nije bilo slučajeva teške hipoglikemije. Incidencija blage hipoglikemije iznosila je 0,286 slučajeva po pacijentu godišnje. U grupama za usporedbu, učestalost blage hipoglikemije bila je 0,029 slučajeva po pacijentu godišnje u liječenju liraglutidom
1,8 mg i 0,129 slučajeva po pacijentu godišnje uz tretman metforminom.
Probavni poremećaji
Većina slučajeva mučnine bila je blaga ili umjerena, privremena i rijetko je vodila do povlačenja terapije.
Kod kombinovanog liječenja lijekom Victoza® i metforminom, mučnina se pojavila barem jednom kod 20,7% pacijenata, a proljev kod 12,6% bolesnika. U kombinaciji s Viktozom® i sulfonilurejom, mučnina se pojavila barem jednom u 9,1% bolesnika, a proliv u 7,9%. Većina slučajeva bila je blaga ili umerena po težini i bila su zavisna od doze.
Kod pacijenata starijih od 70 godina mogu se javiti poremećaji probavnog sistema liječenjem Victoza®.
U bolesnika s blagom oštećenjem bubrežne funkcije (klirens kreatinina od 60-90 ml / min), poremećaji probavnog sustava mogu se češće javljati tijekom liječenja Viktoza®-om.
Povlačenje lijekova
Tijekom dugotrajnih kontroliranih ispitivanja (26 tjedana ili duže), učestalost povlačenja lijeka Viktoza® zbog neželjenih reakcija koje su se desile iznosila je 7,8%, a povlačenje referentnog lijeka 3,4%. Najčešći uzrok toga kod pacijenata koji su primali Victoza® bila je mučnina (2,8%) i povraćanje (1,5%).
Zbog potencijalnih imunogenih svojstava lijekova koji sadrže proteine ili peptide, protutijela protiv liraglutidna mogu se formirati u bolesnika liječenih Victoza®. Otkriveni su u prosječno 8,6% pacijenata. Formiranje antitijela nije bilo povezano sa smanjenjem efikasnosti Victoza®.
Reakcije na mjestu ubrizgavanja
Tijekom dugotrajnih kontroliranih ispitivanja (26 tjedana ili duže), prijavljene su reakcije na mjestu ubrizgavanja Viktoza® kod otprilike 2% bolesnika. Te su reakcije obično bile blage.
Tijekom dugotrajnih kliničkih ispitivanja prijavljeno je nekoliko slučajeva tijekom liječenja Viktozom® (® nije utvrđeno niti isključeno).
Disfunkcija štitne žlezde
Ukupna učestalost disfunkcije štitnjače tokom svih studija (srednja i dugačka) iznosila je 33,5, 30,0 i 21,7 slučajeva na 1000 pacijentskih godina od ukupne izloženosti liraglutida, placeba i uporednih lekova, sa 5,4 , 2.1 i 0.8 slučajeva pripisani su teškim nuspojavama.
U bolesnika liječenih Victoza®-om, tumori štitne žlijezde najčešće su zabilježeni povećani nivo kalcitonina u krvi i gušavi.
Nakon lansiranja lijeka Victoza® na tržište, zabilježene su alergijske reakcije, uključujući urtikariju, osip i svrbež. Zabilježeno je i nekoliko slučajeva anafilaktičkih reakcija s dodatnim simptomima kao što su hipotenzija, palpitacije, dispneja i edemi.
Upotreba tokom trudnoće i dojenja
Nisu dostupni odgovarajući podaci o upotrebi lijeka Viktoza® od trudnica. Studije na životinjama pokazale su reproduktivnu toksičnost (vidjeti odjeljak „Predklinički podaci o sigurnosti“). Potencijalni rizik za ljude nije poznat.
Lijek Viktoza® se ne smije primjenjivati tijekom trudnoće, preporučuje se umjesto njega propisati insulin. Ako pacijent želi zatrudnjeti ili zatrudniti, lijek Victoza ® treba prekinuti.
Period dojenja
Nije poznato da li se liraglutid izlučuje u majčino mlijeko. Studije na životinjama pokazale su da beznačajne količine liraglutida i njegovih usko povezanih strukturnih metabolita dospijevaju u mlijeko. Zbog nedovoljnog iskustva tijekom dojenja, lijek Viktoza® se ne smije koristiti.
Zbog nedostatka podataka, Victoza® se ne preporučuje djeci.
Značajke aplikacije
Victoza® se ne koristi za liječenje bolesnika sa šećernom bolešću tipa 1 ili dijabetičkom ketoacidozom.
Viktoza® nije zamjena za inzulin.
Učinkovitost dodatnog unosa liraglutida kod pacijenata koji se već liječe inzulinom, a nije procijenjena.
Iskustvo liječenja pacijenata s kongestivnim zatajenjem srca I-II klase (prema klasifikaciji njujorške udruge kardiologije - NYHA) je ograničeno, a nema podataka o liječenju bolesnika s kongestivnim zatajenjem srca III-IV klase.
Zbog ograničenog iskustva, ne preporučuje se propisivanje lijeka Viktoza® bolesnicima sa upalnim bolestima crijeva i dijabetičkom gastroparezom.
Upotreba drugih analoga GLP-1 povezana je s rizikom od razvoja pankreatitisa. Postoji veliki broj izvještaja o akutnom pankreatitisu. Bolesnike treba obavijestiti o karakterističnim simptomima akutnog pankreatitisa (uporni, jaki bolovi u trbušnoj šupljini). Ako se sumnja na pankreatitis, potrebno je prekinuti liječenje Viktozom® i drugim provokativnim lijekovima.
Tokom kliničkih ispitivanja, uočene neželjene reakcije štitne žlijezde su povećanje razine kalcitonina u krvi, gušavi i tumora, posebno kod pacijenata sa postojećim bolestima štitnjače (vidjeti odjeljak „Neželjene reakcije“).
Pacijenti liječeni lijekom Victoza® imali su simptome dehidracije, uključujući oštećenje bubrežne funkcije i akutno zatajenje bubrega.
Pacijente koji su predodređeni za lijek Victoza® treba upozoriti na mogućnost dehidracije zbog poremećaja probavnog sustava i na potrebu poduzimanja mjera opreza za dehidraciju.
U bolesnika koji primaju lijek Viktoza® istovremeno sa sulfonilurejom, rizik od razvoja hipoglikemije se povećava (vidjeti dio „Neželjene reakcije“). Rizik od hipoglikemije može se smanjiti smanjenjem doze sulfonilureje.
Mogućnost utjecaja na brzinu reakcije tijekom vožnje vozila ili drugih mehanizama
Ispitivanja utjecaja lijeka Victoza® na sposobnost upravljanja vozilima i drugih mehanizama nisu provedena. Pacijente treba savjetovati da poduzmu mjere za sprečavanje pojave hipoglikemije za vrijeme vožnje vozila ili drugog mehanizma, posebno kada koriste Victoza® zajedno sa sulfonilurejom.
Interakcija s drugim lijekovima i druge vrste interakcija .
In vitro liraglutid je pokazao vrlo nizak potencijal farmakokinetike drugih aktivnih tvari čija je izmjena povezana s citokromom 450 kao i vezanje za proteine plazme.
Liraglutid uzrokuje malo kašnjenje u pražnjenju želuca, može utjecati na apsorpciju lijekova koji se istovremeno koriste unutar.
Liraglutide nije promijenio ukupnu izloženost paracetamola nakon jedne doze od 1000 mg. Maksimalna koncentracija paracetamola (C maks ) smanjen za 31%, a vrijeme za postizanje maksimalne koncentracije (t maks ) povećao se na 15 minuta. Uz istodobnu upotrebu paracetamola, nije potrebno prilagođavanje doze.
Atorvastatin Liraglutid nije promijenio ukupnu izloženost atorvastatina klinički značajne razine nakon njegove jednostruke doze u dozi od 40 mg. S tim u vezi, uz istodobnu upotrebu Viktozoy® doza atorvastatina nije potrebna. Primijenjeno istodobno s liraglutidom C maks atorvastatin se smanjio za 38%, a t maks povećan od 1:00 do 3:00.
Griseofulvin Liraglutid nije promijenio ukupnu izloženost grizeofulvinu nakon pojedinačne doze od 500 mg. C maks porastao je za 37%, dok t maks nisu se promijenile. Prilagođavanje doze kod upotrebe griseofulvina i drugih spojeva niskog korijena s visokom propusnošću nije potrebno.
Lisinopril i digoksin
Nakon jedne injekcije 20 mg lizinoprila ili 1 mg digoksina u kombinaciji s liraglutidom, zabilježeno je smanjenje površine ispod krivulje koncentracije (AUC) ovih lijekova za 15%, odnosno 16%, s C maks smanjena za 27%, odnosno 31%. T maks lizinopril je porastao sa 6:00 na 8:00, dok je digoksin povećan sa 1:00 na 1,5 sat. Na osnovu ovih rezultata, dok koristite liraglutid, prilagodba doze lizinoprila ili digoksina nije potrebna.
Uz upotrebu jedne doze oralnih kontraceptiva, liraglutid smanjuje C maks etinil estradiol ili levonorgestrel za 12%, odnosno 13%, i t maks povećao za 1,5 sata. Ovo nije pokazalo klinički učinak na ukupnu izloženost etinil estradiola ili levonorgestrela, što upućuje na to da istodobna primjena liraglutida neće utjecati na kontracepcijski učinak etinil estradiola i levonorgestrela.
Varfarin i drugi derivati kumarina
Nisu provedena ispitivanja interakcije lijekova. Na početku liječenja Viktozom® za bolesnike koji primaju varfarin ili druge kumarinske derivate preporučuje se često praćenje INR-a (međunarodni normalizirani omjer).
U bolesnika sa stabiliziranim šećernom bolešću tipa 2 s istodobnom primjenom inzulina, detemir (5 U / kg) i liraglutid (1,8 mg) nisu pokazali znakove farmakokinetičke i farmakodinamičke interakcije.
Farmakokinetika
Nakon subkutane primjene, apsorpcija liraglutida je spora, Tmaks (vrijeme postizanja maksimalne koncentracije) u plazmi je 8-12 sati. Cmaks (maksimalna koncentracija) u plazmi nakon primjene pojedinačne doze od 0,6 mg iznosi 9,4 nmol / L. Kada koristite dozu od 1,8 mg prosječne Css (ravnotežna koncentracija) u plazmi doseže približno 34 nmol / L. Izloženost tvari povećava se proporcionalno dozi. Koeficijent varijacije unutar pojedinca za AUC (površina ispod krivulje koncentracija-vrijeme) nakon primjene liraglutida u jednoj dozi je 11%. Apsolutna bioraspoloživost je oko 55%.
Seeming Vd (volumen distribucije) liraglutida u tkivima s potkožnim načinom davanja je 11-17 l, prosječna vrijednost Vd nakon intravenske primjene - 0,07 l / kg. Primijećeno je značajno vezanje liraglutida s proteinima plazme (> 98%).
Metabolizam liraglutida odvija se poput velikih proteina, ne sudjelujući kao put za izlučivanje bilo kojeg određenog organa. 24 sata nakon primjene jedne doze, nepromijenjena supstanca ostaje glavna komponenta plazme. U plazmi su otkrivena dva metabolita (≤ 9 i ≤ 5% ukupne doze).
Nepromijenjeni liraglutid nakon primjene doze 3 H-liraglutida u urinu ili izmetu nije određen. Samo mali dio metabolita povezanih sa supstancom izlučuje se putem bubrega ili creva (6, odnosno 5%). Nakon potkožne primjene jedne doze liraglutida, prosječni klirens iz tijela je približno 1,2 l / h uz eliminaciju T1/2 oko 13 sati.
Oblik za puštanje i pakiranje
3 ml lijeka u ulošku stakla 1 hidrolatne klase, zabrtvljenom s diskom brombutil gume / poliizoprena s jedne strane i klipom brombutilne gume s druge strane. Uložak je zatvoren u plastičnoj olovci za jednokratnu upotrebu za višestruku injekciju.
2 plastične jednokratne štrcaljke za višestruke injekcije zajedno s uputama za medicinsku upotrebu na državnom i ruskom jeziku smještene su u pakiranje od kartona.
Svaka olovka za špricu (3 ml) sadrži 30 doza od 0,6 mg, 15 doza od 1,2 mg ili 10 doza od 1,8 mg liraglutida.
Indikacije za upotrebu
Prema uputama, Viktoza se koristi za dijabetes tipa 2 u kombinaciji sa dijetom i vježbanjem za postizanje glikemijske kontrole.
Mogući načini upotrebe lijeka:
- monoterapija
- kombinirana terapija s jednim ili više oralnih hipoglikemijskih lijekova (tiazolidindioni, sulfonilureje, metformin) u bolesnika koji nisu uspjeli postići odgovarajuću kontrolu glikemije tijekom prethodne terapije,
- kombinirana terapija bazalnim inzulinom kod pacijenata koji nisu uspjeli postići adekvatnu kontrolu glikemije koristeći Victoza u kombinaciji s metforminom.
Uputa za upotrebu Victoza: metoda i doziranje
Victozu treba davati subkutano u abdomen, rame ili bedra jednom dnevno, bez obzira na obroke. Mjesto i vrijeme ubrizgavanja mogu se promijeniti bez prilagođavanja doze, međutim, poželjno je davati lijek u približno isto doba dana, što je za pacijenta najpovoljnije.
Za poboljšanje gastrointestinalne tolerancije preporučuje se liječenje dnevnom dozom od 0,6 mg. Nakon najmanje sedmice, doza se povećava na 1,2 mg. Ako je potrebno, kako bi se postigla najbolja kontrola glikemije, uzimajući u obzir kliničku učinkovitost Victoze, moguće je povećanje doze na 1,8 mg najmanje tjedan dana kasnije. Primjena većih doza se ne preporučuje.
Lijek se može propisati uz kontinuiranu terapiju metforminom ili kombiniranu terapiju metforminom u kombinaciji s tiazolidindionom. Doze ovih potonjih ne moraju se prilagođavati.
Victoza se može dodati postojećoj terapiji derivata sulfoniluree ili kombiniranoj terapiji metforminom u kombinaciji sa derivatima sulfoniluree. U tom slučaju, da bi se minimizirao rizik od razvoja neželjene hipoglikemije, dozu derivata sulfonilureje treba smanjiti.
Victoza se može dodati i bazalnom inzulinu, ali da bi se smanjio rizik od hipoglikemije, potrebno je smanjiti dozu inzulina.
U slučaju da nedostaje doza:
- ako nije prošlo više od 12 sati, morate unijeti propuštenu dozu što je prije moguće,
- ako je prošlo više od 12 sati, sljedeću se dozu mora primijeniti sljedeći dan u zakazano vrijeme, tj. nije potrebno nadoknaditi dozu unošenjem dodatne ili udvostručene doze.
Smjernice za upotrebu lijeka
Svaka olovka za šprice dizajnirana je za individualnu upotrebu.
Lijek treba davati iglama dužine do 8 mm i debljine do 32G (nisu uključene, stoga se kupuju zasebno). Olovke za špriceve kombinovane su sa jednokratnim injekcijskim iglama NovoTvist i NovoFayn.
Victoza se ne smije davati ako rastvor izgleda drugačije od bistre, gotovo bezbojne ili bezbojne tekućine.
Ne možete unijeti lijek ako je prošao zamrzavanje.
Ne čuvajte olovku za štrcaljku sa pričvršćenom iglom. Nakon svake injekcije mora se odbaciti. Ova mjera sprječava curenje, zagađenje i infekciju lijeka, a također garantuje tačnost doziranja.
Uslovi skladištenja
Čuvati na 2 ° C do 8 ° C (u hladnjaku). Ne smrzavajte se.
Za olovku štrcaljke u upotrebi: koristite u roku od 1 meseca. Čuvati na temperaturi koja ne prelazi 30 ° C ili od 2 ° C do 8 ° C (u hladnjaku). Ne smrzavajte se. Ne čuvati sa pričvršćenom iglom. Pokrijte olovku za šprice poklopcem da biste je zaštitili od svetlosti.
Čuvajte van dohvata djece!
Vodič za upotrebu i odlaganje
Victoza® se ne može koristiti ako izgleda drugačije od bistre i bezbojne ili gotovo bezbojne tečnosti.
Victoza® se ne može koristiti ako je bio smrznut.
Victoza® se može davati iglama dužine do 8 mm i debljine do 32G. Olovka za štrcaljku namenjena je upotrebi u kombinaciji sa NovoFine® ili NovoTvist® injekcijskim iglama za jednokratnu upotrebu.
Igle za ubrizgavanje nisu u kompletu.
Pacijenta treba obavijestiti da upotrijebljenu iglu treba odbaciti nakon svake injekcije, kao i da se špric olovke sa priloženom iglom ne može pohraniti. Takva mjera spriječit će kontaminaciju, infekciju i curenje lijeka iz olovke štrcaljke i garantovati precizno doziranje.