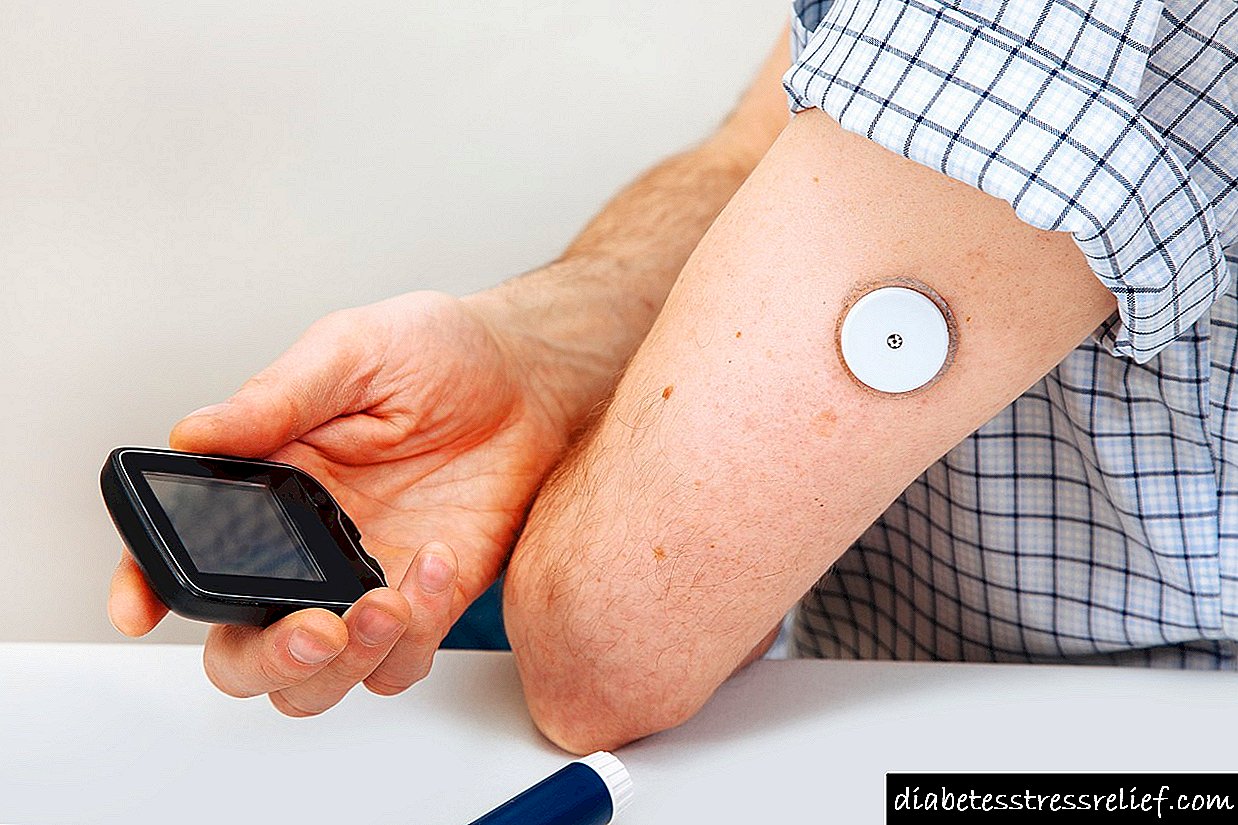
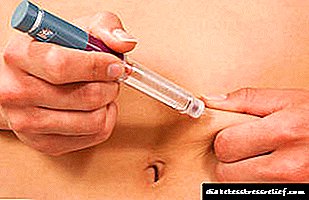
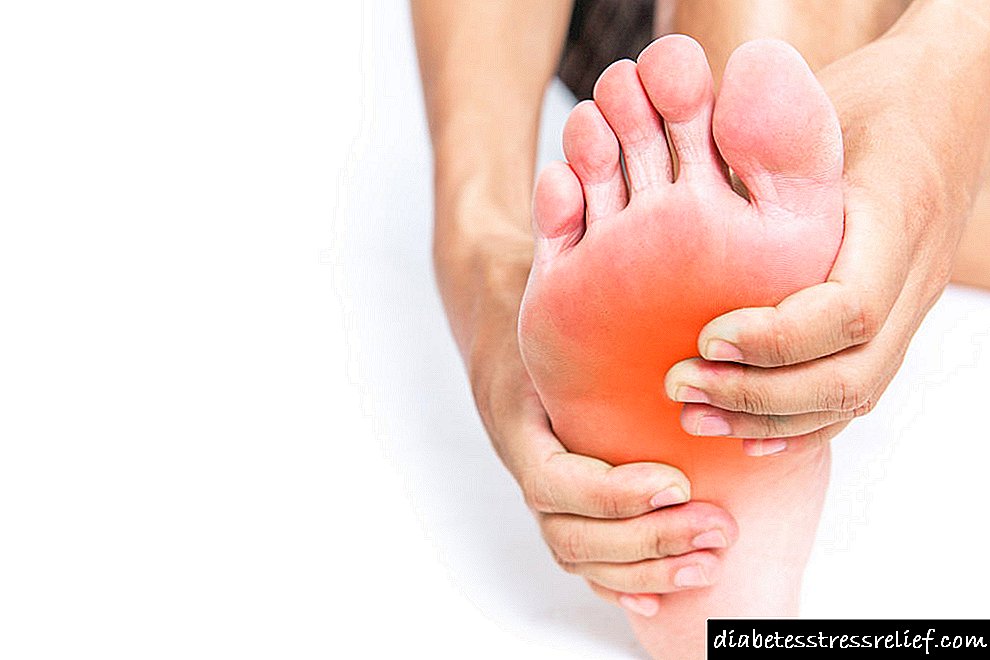
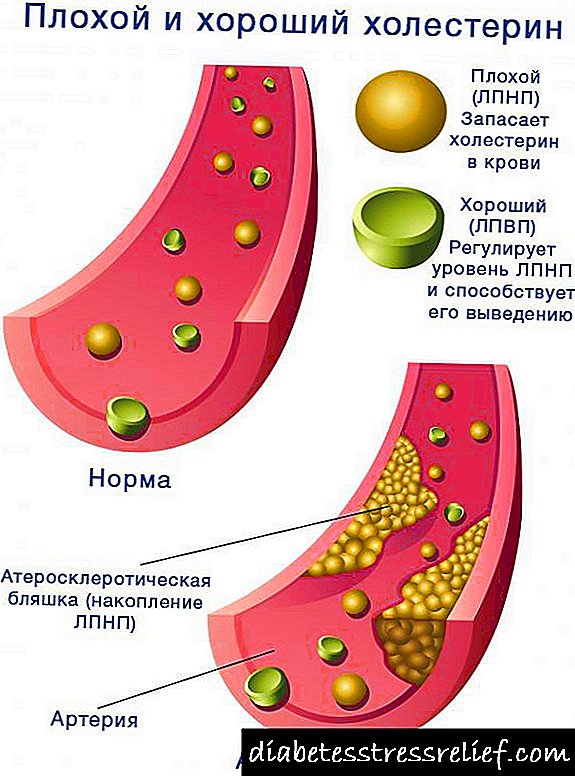
Glavne nuspojave glukokortikoida
Dugogodišnje iskustvo sa glukokortikoidnim lekovima kod različitih bolesti kod dece otkrilo je ne samo pozitivne, već i negativne aspekte ove metode terapije. Utvrđeno je da su kod nekih pacijenata nuspojave privremene i blago izražene prirode i nestaju bez traga.
Kod druge djece, nakon ukidanja glukokortikoidnog sredstva, nastale komplikacije, ponekad vrlo teške, traju više godina, a ponekad i tijekom života. Priroda i težina nuspojava i komplikacija ovise o dnevnoj dozi i trajanju tijeka liječenja glukokortikosteroidnim lijekovima, dobi djeteta i individualnim karakteristikama reaktivnosti njegovog tijela.
Mehanizmi nuspojava koje uzrokuju glukokortikosteroidi su složeni, jer ovi lijekovi upadaju u sve aspekte vitalne aktivnosti djetetovog tijela. Međutim, nesumnjivo se može govoriti o toksičnim i alergijskim efektima ovih lijekova, o njihovoj sposobnosti da grubo naruše stanje imuniteta, uzrokuju razaranje tkiva i inhibiraju regeneracijske procese u njima, značajno poremetijući metabolizam. Neželjene reakcije i komplikacije u liječenju djece glukokortikosteroidima mogu biti sljedeće.
1.Jedna od čestih manifestacija hiperkortizma lijekova umjetno stvorenog u dječjem tijelu je Cushingoid sindrom: debljanje sa simptomima osebujne pretilosti (zaokruživanje lica, pretjerano taloženje masti na licu, vratu, ramenima, trbuhu) u kombinaciji s hipertrikozom, znojenjem ili suhom kožom, njenom pigmentacijom, povećanim vaskularnim obrascem kože, pojavom akni i strija.
Pojačano taloženje masti (gojaznost muškog tipa) povezano je s kataboličkim učinkom glukokortikosteroidnih lijekova, pojačanim procesima glukoneogeneze i pretvorbom ugljikohidrata u masti. Inhibicija procesa mobilizacije masti koje potiču hormon rasta takođe je važna.
2. Česta neželjena reakcija na primjenu glukokortikosteroida je takozvani steroidni gastritis, koji se očituje pogoršanjem apetita, žgaravicom, mučninom, ponekad povraćanjem, kiselim lučenjem, bolom u epigastričnoj regiji.
Moguća je i komplikacija u obliku erozije i čira na želucu i dvanaesniku (mogu se javiti i u tankom i debelom crijevu). Čir na želucu i crijevima ponekad je kompliciran krvarenjem i perforacijom. Treba napomenuti da čir na želucu i crijevima u početnim fazama njihovog nastanka može biti asimptomatski, a znak njihovog postojanja je pozitivna reakcija na okultnu krv u izmetu.
Češće se gastrointestinalne komplikacije pojavljuju nakon uzimanja glukokortikosteroidnih lijekova iznutra, mada njihov razvoj nije isključen uz parenteralnu primjenu ovih lijekova. Pojava ulceroznog procesa najvjerojatnija je prilikom propisivanja prednizona i prednizona, posebno u kombinaciji s drugim ulcerogenim agensima (imunosupresivi, acetilsalicilna kiselina, tetraciklini itd.).
Ostali faktori doprinose razvoju čira:
· Uzimanje glukokortikosteroida pre jela,
Dugotrajno davanje velikih doza ovih lijekova bez prekida u liječenju,
· Nepridržavanje ishrane tokom terapije glukokortikosteroidima (unos začinjene i nadražujuće hrane, začina, hladne ili tople hrane itd.)
Glukokortikosteroidi uzrokuju stvaranje čir na želucu i crijevima zbog sljedećih razloga:
· Povećavaju kiselost i lučenje želudačnog soka, a istovremeno remete stvaranje sluzi, koja štiti sluznicu želuca i creva od štetnih efekata (inhibira se sinteza polisaharida koji čine sluznicu želudca i creva),
· Glukokortikosteroidi slabe procese zarastanja mikro- i makro ulkusa želuca i creva, odnosno pod njihovim uticajem se sprečava proliferacija ćelija žlezdanog i vezivnog tkiva zidova ovih organa. Asimptomatski (bezbolni) tijek ulceroznog procesa objašnjava se činjenicom da se ulceracija pojavljuje na pozadini protuupalnog učinka glukokortikosteroidnih lijekova.
3. U procesu uzimanja glukokortikosteroidnih lijekova može se primijetiti pogoršanje žarišne infekcije (tonzilitis, sinusitis, propadanje zuba, holecistitis i drugi), generalizirati zarazni proces. Opisani su slučajevi upale pluća i plućne suppuracije autoinfektivnog porijekla, pogoršanja hroničnih bolesti (hepatitis, holecistitis, pankreatitis, tuberkuloza i drugi).
Napominje se da imenovanje glukokortikosteroida izaziva teže tijek virusnih infekcija kod djece, a dramatično pogoršava učinkovitost vakcinacije. Gore navedene nuspojave objašnjavaju se sposobnošću glukokortikosteroida da suzbijaju sistemske i lokalne obrambene reakcije.
4. U liječenju glukokortikosteroidima moguće su promjene u mentalnoj i emocionalnoj sferi: emocionalna labilnost, logorreja, psihomotorna uznemirenost, poremećaj spavanja. Te su promjene kod djece reverzibilne.
5. Česta neželjena reakcija s terapijom glukokortikosteroidima je porast krvnog tlaka. Nakon otpusta iz bolnice prolazi arterijska hipertenzija kod pacijenata, mada kod neke djece porast krvnog pritiska za 15 - 20 mm RT. Čl. traje 1 do 3 godine ako nema pritužbi (A. V. Dolgopolova, N. N. Kuzmina, 1963).
Mehanizam arterijske hipertenzije u hiperkortikaciji lijekova ostaje nejasan. Češće se takva reakcija bilježi u prepubertalnom i pubertetskom dobu.
6. Neki glukokortikosteroidi (kortizon, hidrokortizon, prednizon, prednizon) imaju sposobnost zadržavanja natrijuma i vode u bolesnikovom tijelu, što doprinosi pojavi edema i povećanju tjelesne težine. Takvi glukokortikosteroidni lijekovi kao deksametazon, triamcinolon, metilprednizolon ne odlažu natrijum i vodu.
7.Uz masivnu i dugotrajnu terapiju glukokortikosteroidima kod djevojčica adolescenata, često se primjećuju endokrini poremećaji: kašnjenje u pojavi prve menstruacije, njihova nepravilnost, kada su već uspostavljene. Treba se složiti s tim i bez strogih indikacija ne dajete ove lijekove djevojčicama u pubertetskom razdoblju, otkažite ih kada se pojave prvi znakovi ovih negativnih pojava.
8. Literatura pruža dokaze da pod utjecajem dugotrajne primjene glukokortikosteroidnih lijekova može doći do usporavanja rasta djetetovog tijela. Taj se fenomen objašnjava inhibicijskim učinkom glukokortikosteroida na proizvodnju hormona rasta hipofize i stvaranjem somatomedina u jetri, porastom kataboličkih procesa u tkivima, uključujući kosti.
9. U djetinjstvu se dijabetes melitus može razviti pod utjecajem glukokortikosteroida iz predijabetesa.
Mehanizam nastanka steroidnog dijabetesa povezan je s karakteristikama djelovanja glukokortikosteroidnih lijekova na metabolizam ugljikohidrata: inhibiraju rad izolacijskog aparata gušterače, podstiču proizvodnju proteina plazme koji vežu inzulin, aktiviraju proces stvaranja glukoze iz aminokiselina i istovremeno slabe iskorištavanje ugljikohidrata u tkivima.
U konačnici se razvijaju hiperglikemija i glukozurija, a u djece sa nasljednom ranjivošću otočnog aparata - dijabetes. Kod većine bolesnika nakon ukidanja glukokortikosteroida metabolizam ugljikohidrata se normalizira. Deksametazon može izazvati posebno izražene poremećaje metabolizma ugljikohidrata, manje nego triamcinolon, metilprednizolon, prednizolon, prednizon. Minimalna dijabetogenost je karakteristična za kortizon i hidrokortizon.
10. Česta neželjena reakcija djetetovog tijela na primjenu glukokortikosteroida je povećana izlučivanje kalija u urinu i razvoj hipokalemičkog sindroma.
Znakovi potonjeg: osjećaj slabosti, nelagode, gubitak mišićnog tonusa i snage (ponekad pareza udova), slabljenje funkcije miokarda, srčana aritmija, mučnina, povraćanje, zatvor.
Mogućnost razvoja hipokalemijskog sindroma povećava se uz primjenu glukokortikosteroida u kombinaciji sa srčanim glikozidima i diureticima, uz zanemarivanje dijeta s kalijem i nedovoljnom nadoknadom farmakogenih gubitaka kalija zbog dodatne primjene kemoterapijskih lijekova koji sadrže kalij.
11. Nakupljeno je mnogo kliničkih opažanja koja ukazuju na negativne efekte glukokortikosteroidnih lekova na skeletni sistem deteta. Steroidna osteopatija izražava se pojavom osteoporoze pretežno dugih tubularnih kostiju, rebara i tijela kralježaka. Često je razvoj epifizne hrskavice poremećen, ponekad se pojave znakovi aseptične nekroze kostiju.
Vrlo ozbiljna komplikacija je brevispondilija: stvaranje ribljih kralježaka (uslijed uništenja tijela kralježaka i intervertebralnih diskova), praćeno mogućim povredom živčanih korijena, prijelomom kralježnice, kompresijom leđne moždine.
Steroidna osteopatija rezultat je grubih kršenja sinteze proteinskih struktura koštanog tkiva (smanjenje količine kolagena, mukopolisaharida, heksosamina), pojačanog procesa reapsorpcije kalcija iz koštanog tkiva i prekomjernog izlučivanja njega i fosfora u urinu. Reparativni procesi u koštanom tkivu pacijenata sa steroidnom osteopatijom karakteriziraju letargija i trajanje.
12. Kod nekih bolesnika miopatija se razvija pod utjecajem glukokortikosteroidnih lijekova.
Njeni simptomi: mišićna slabost (uglavnom u proksimalnim donjim ekstremitetima i mišićima trupa), hipotenzija, smanjeni tetivni refleksi. Na pregledu možete primetiti znakove hipertrofije mišića, posebno donjih ekstremiteta (povećava se sadržaj glikogena u mišićima). Dokazano je kršenje strukture živčano-mišićnih sinapsi. Triamcinolon koji sadrži fluor često uzrokuje miopatiju. Steroidna miopatija nakon povlačenja lijeka postepeno nestaje, a šupljina se vraća i funkcija i struktura mišića.
13. Primjena glukokortikosteroida (posebno u slučajevima dugotrajne primjene ogromnih doza lijekova) prepun je opasnosti od komplikacija od vidnog organa u obliku zamućenja leće i glaukoma. Promjene sočiva mogu postati ireverzibilne zbog ukapavanja vodenog humora, sabijanja stražnjeg dijela. Glaukom u djetinjstvu je rijedak.
14. Iako su glukokortikosteroidni lijekovi snažan terapeutski faktor kod alergija, u nekim slučajevima oni sami stvaraju alergijske reakcije, sve do anafilaktičkog šoka. Takve se reakcije često javljaju ponavljanim tečajevima terapije glukokortikosteroidima i manifestuju se u obliku urtikarije, Quinckeovog edema, multiformnog eritema, svrbeža kože i drugih znakova.
15. Dugotrajna primjena glukokortikosteroidnih lijekova i rezultirajuće stanje farmakogenog hiperkortizma prepun je opasnosti od inhibicije funkcije kortikalnog sloja nadbubrežne žlijezde i kompenzacijskog restrukturiranja hipotalamičko-ginefizičko-nadbubrežnog sustava.
U skladu s tim, pri naglom povlačenju lijeka, sindrom odvikavanja može se razviti u obliku napada jake slabosti, slabosti, glavobolje, smanjene mentalne i fizičke sposobnosti i umjerenog porasta tjelesne temperature.
Sindrom povlačenja posebno je opasan u slučajevima kada se primjena velikih doza glukokortikosteroida zaustavi bez prethodne pripreme pacijentovog tijela, naime, bez postepenog smanjivanja dnevne doze lijeka, uvođenja hemoterapijskih sredstava koja stimulišu funkciju kore nadbubrežne žlijezde.
Dakle, grupu glukokortikosteroidnih lijekova karakteriziraju ne samo njegovi snažni terapeutski učinci na pacijentovo tijelo, već i mnoge negativne pojave, čija ozbiljnost i suština ovise i o samom lijeku, načinu njegove upotrebe, dobi i spolu djeteta i drugim faktorima, nažalost još nije izučeno.
Farmakološka terapija za HA može biti intenzivna (kratkotrajna), ograničena (nekoliko dana ili mjeseci) i dugotrajna (liječenje nekoliko mjeseci, godina ili čak doživotno).
Niste pronašli ono što tražite? Koristite pretragu:
Nuspojave sistemskih glukokortikoida
Sadržaj
Nuspojave
■ Inhibicija funkcije i atrofija kore nadbubrežne korekcije, steroidna zavisnost, „sindrom povlačenja“ (pogoršanje osnovne bolesti, nadbubrežna insuficijencija). Dugotrajna terapija sistemskim glukokortikoidima, posebno provedena bez vodeći računa o fiziološkim cirkadijanskim ritmovima njihove sekrecije, dovodi do inhibicije i atrofije nadbubrežne kore. Za potpunu inhibiciju nadbubrežne kore kod odraslog pacijenta, dnevna doza egzogenog glukokortikoida treba iznositi 10-20 mg u odnosu na prednizon. Smanjenje funkcije kore nadbubrežne žlijezde započinje između 4. i 7. dana svakodnevne primjene srednjih doza glukokortikoida kada se propisuju ujutro i od 2. dana kada ih se propisuje uveče. Ova nuspojava je najkarakterističnija za oralne glukokortikoide i depo-pripravke dugog djelovanja. Za vraćanje normalne sekretorne funkcije kore nadbubrežne kosti potrebno je najmanje 6–9 mjeseci, a njen adekvatan odgovor na stres je do 1-2 godine.
■ Stanjivanje kože, strija, ćelavost.
■ Osteoporoza, prelomi i aseptična nekroza kostiju, usporavanje rasta. Osteoporoza se razvija kod 30-50% pacijenata i najozbiljnija je komplikacija terapije glukokortikoidima. To je posljedica njihovog negativnog utjecaja na formiranje koštanog tkiva i aktiviranja njegove resorpcije. Često se razvija kod žena u postmenopauzalnom periodu. U pravilu osteoporoza zahvaća središnje dijelove skeleta (kralježnicu, zdjelične kosti, rebra) i postepeno se širi na periferne kosti (ruke, stopala i dr.) Njegove kliničke manifestacije su bol u kralježnici i zglobovima kuka, smanjen rast i prijelomi kralježnice (donji torakalni i lumbalni dio odeljenja), rebra, vrat femura, koji nastaju usled manjih povreda ili spontano. Za liječenje ove komplikacije koriste se kalcijumski pripravci, vitamin D3, kalcitonin i bisfosfonati. Trajanje takve terapije trebalo bi biti nekoliko godina.
• miopatija, gubitak mišića, distrofija miokarda. Steroidne miopatije očituju se slabošću i atrofijom skeletnih mišića, uključujući respiratorne mišiće (interkostalni mišići, dijafragma), što doprinosi razvoju zatajenja disanja. Najčešće ovu komplikaciju izaziva triamcinolon. Mehanizam razvoja miopatije povezan je s negativnim učinkom glukokortikoida na metabolizam proteina i minerala. Za njihovo liječenje koriste se anabolički steroidi i pripravci s kalijem.
■ Hipokalemija, zadržavanje natrijuma i vode, edemi su manifestacije mineralokortikoidnih efekata glukokortikoida.
■ Povećanje krvnog pritiska može se primjetiti kod pacijenata koji dugo uzimaju glukokortikoide. Nastaje zbog povećane osjetljivosti vaskularne stijenke na kateholamine, zadržavanje natrijuma i vode.
■ Oštećenja vaskularnog zida sa razvojem „steroidnog vaskulitisa“ često nastaju fluoriranim lijekovima (deksametazon i triamcinolon). Karakterizira ga povećana vaskularna propustljivost. Manifestira se krvarenjem u koži podlaktica, sluznicom usne šupljine, konjuktivom očiju, epitelom gastrointestinalnog trakta. Za liječenje se koriste vitamini C i P, kao i anti-bradikinin.
■ Povećanje koagulabilnosti krvi može dovesti do stvaranja krvnih ugrušaka u dubokim venama i tromboembolije.
■ Usporavanje regeneracije tkiva zbog antianaboličkog i kataboličkog efekta na metabolizam proteina - smanjenje sinteze proteina iz aminokiselina, pojačavanje razgradnje proteina.
■ Steroidni čir na želucu i crevima, gastrointestinalno krvarenje. Steroidni čirevi često su asimptomatski ili asimptomatski, manifestujuće krvarenje i perforaciju. Zbog toga bolesnike koji duže vrijeme primaju oralne glukokortikoide treba periodično pregledavati (fibroezofagogastroduodenoskopija, test okultne krvi u fekalu). Mehanizam ulcerogenog djelovanja glukokortikoida povezan je s njihovim kataboličkim učinkom i suzbijanjem sinteze prostaglandina i sastoji se u povećanju izlučivanja klorovodične kiseline, smanjenju stvaranja sluzi i inhibiranju regeneracije epitela. Ovu komplikaciju češće uzrokuje prednizon.
■ Pankreatitis, masna jetra, gojaznost, hiperlipidemija, hiperholesterolemija, embolija masti rezultat su anaboličkog učinka glukokortikoida na metabolizam masti - povećane sinteze triglicerida, masnih kiselina i holesterola, preraspodjele masti.
■ Povećana ekscitabilnost CNS-a, nesanica, euforija, depresija, psihoza, simptomi meningizma, napadaji kod pacijenata sa epilepsijom.
■ Posteriorna subkapsularna katarakta, glaukom, egzoftalmos.
■ Steroidni dijabetes, hiperglikemija. Glukokortikoidi povećavaju apsorpciju ugljikohidrata iz gastrointestinalnog trakta, pojačavaju glukoneogenezu, smanjuju aktivnost inzulina i hekokinaze i smanjuju osjetljivost tkiva na inzulin i njihovu upotrebu glukoze. Za liječenje steroidnog dijabetesa koriste se dijeta ograničena ugljikohidratima, oralni hipoglikemijski lijekovi i inzulin.
■ Kršenje menstrualnog ciklusa, seksualne funkcije, odgođeni seksualni razvoj, hirzutizam, poremećen razvoj fetusa povezani su sa smanjenjem proizvodnje spolnih hormona.
■ Suzbijanje imuniteta, pogoršanje hroničnih zaraznih i upalnih procesa, uključujući tuberkulozu, sekundarnu infekciju, generalizaciju lokalne infekcije. U pravilu su zarazne komplikacije asimptomatske zbog protuupalnog učinka glukokortikoida. Karakterističan je razvoj kandidijaze usne šupljine i ždrijela.
■ Cushingov sindrom (mobilizacija masti iz potkožnog masnog tkiva udova, prekomerno taloženje masti na licu, vratu, ramenom pojasu i trbuhu, hipertrihoza, strije, akne, oslabljena tolerancija na glukozu itd.).
■ Hematološke promene.
■ Manifestira se neutrofilnom leukocitozom bez pomaka leukocitne formule ulijevo. Vjeruje se da nastaju zbog stimulativnog učinka steroida na granulopoezu.
Sprečavanje komplikacija
■ Upotreba povremenog (naizmeničnog) režima lečenja.
■ Upotreba sistemskih glukokortikoida u minimalnoj potrebnoj dozi. Zbog toga, kod bronhijalne astme, njihovu primjenu treba kombinirati s primjenom inhaliranih glukokortikoida u kombinaciji s dugo djelujućim β2-adrenergičkim agonistima, teofilinom ili antileukotrienskim lijekovima.
■ Davanje glukokortikoida u skladu sa fiziološkim dnevnim ritmom lučenja kortizola.
■ Upotreba prehrane bogate proteinima i kalcijumom, uz ograničenje lako probavljivih ugljikohidrata, soli (do 5 g dnevno) i tečnosti (do 1,5 litara dnevno).
■ Uzimanje tableta glukokortikoida nakon obroka radi smanjenja ulcerogenog učinka.
■ Eliminacija pušenja i zloupotrebe alkohola.
■ Umerena ne-traumatična vežba.
Pojam glukokortikoida, njihova upotreba kao lijekova, klasifikacija po strukturi i djelovanju. Načini regulacije sinteze i izlučivanja hormona nadbubrežne kore Mehanizam djelovanja glukokortikoida, glavni sporedni efekti njihove upotrebe.
| Heading | Medicina |
| Pogled | apstraktno |
| Jezik | Ruski |
| Datum dodavanja | 22.05.2015 |
| Veličina datoteke | 485.1 K |

Podnošenje vašeg dobrog rada u bazu znanja je jednostavno. Upotrijebite donji obrazac
Studenti, diplomirani studenti, mladi naučnici koji u svom radu i radu koriste bazu znanja biće vam vrlo zahvalni.
Objavljeno http://www.allbest.ru/
Ministarstvo zdravlja Ukrajine
Zaporizhzhya State Medical University
Zavod za farmakologiju i medicinski recept
Predmet: "Farmakologija"
O temi: „Nuspojave glukokortikoida“
Završena: student 3. godine
Saiko Roman Eduardovich
1. Klasifikacija glukokortikoida
2. Mehanizam djelovanja glukokortikoida
3. Upotreba glukokortikoida
4. Glavne nuspojave glukokortikoida
5. Prevencija nuspojava glukokortikoida
Spisak referenci
1.Klasifikacija glukokortikoidau
Glukokortikoidi su steroidni hormoni sintetizovani u kore nadbubrežne žlijezde. Prirodni glukokortikoidi i njihovi sintetički analozi koriste se u medicini za nadbubrežnu insuficijenciju. Pored toga, neke bolesti koriste protivupalna, imunosupresivna, antialergijska, anti-šok i druga svojstva ovih lekova.
Početak upotrebe glukokortikoida kao lijekova (PM) seže u četrdesete godine. XX vek. U kasnim 30-ima. prošlog veka, pokazalo se da se u kore nadbubrežne energije stvaraju hormonska jedinjenja steroidne prirode. 1937. godine, mineralokortikoidni deoksikortikosteron izoliran je iz kore nadbubrežne žlijezde, 40-ih. - glukokortikoidi kortizon i hidrokortizon. Širok spektar farmakoloških učinaka hidrokortizona i kortizona unaprijed je odredio mogućnost njihove primjene kao lijekova. Ubrzo je izvršena njihova sinteza.
Glavni i najaktivniji glukokortikoid formiran u ljudskom tijelu je hidrokortizon (kortizol), ostali manje aktivni su kortizon, kortikosteron, 11-deoksikortizol, 11-dehidrokortikosteron.
Proizvodnja hormona nadbubrežne žlijezde je pod nadzorom središnjeg živčanog sustava i usko je povezana s funkcijom hipofize (vidjeti Sliku 2). Adrenokortikotropni hormon hipofize (ACTH, kortikotropin) je fiziološki stimulator kore nadbubrežne žlijezde. Kortikotropin pojačava stvaranje i lučenje glukokortikoida. Potonji zauzvrat utječu na hipofizu, inhibirajući proizvodnju kortikotropina i tako smanjuje daljnju stimulaciju nadbubrežne žlijezde (po principu negativne povratne informacije). Produljena primjena glukokortikoida (kortizona i njegovih analoga) u organizam može dovesti do inhibicije i atrofije nadbubrežne kore, kao i do inhibicije stvaranja ne samo ACTH, već i gonadotropnih i štitnjače-stimulirajućih hormona hipofize.
Sl.Klasifikacija glukokortikoida i metode za njihovu upotrebu
Sl.Načini regulacije sinteze i izlučivanja hormona nadbubrežne kore
Od 50-ih godina prošlog vijeka glukokortikoidi su zauzimali važno mjesto u raznim oblastima medicine i, prije svega, u terapijskoj praksi. Sinteza oblika glukokortikoida za intravensku i intramuskularnu primjenu značajno je proširila mogućnosti terapije glukokortikoidima. U proteklih 15-20 godina, naše ideje o mehanizmima djelovanja glukokortikoida znatno su se proširile, a došlo je i do ozbiljnih promjena u taktizi upotrebe glukokortikoida, uključujući doziranje, načine primjene, trajanje upotrebe i kombinacije s drugim lijekovima.
Primjena glukokortikoida u kliničkoj praksi datira iz 1949. godine kada je prvi put zabilježen odličan kratkoročni učinak kortizona kod pacijenata s reumatoidnim artritisom. 1950. godine ista istraživačka skupina izvijestila je o dobrim rezultatima liječenja reumatoidnog artritisa, reumatizma i drugih reumatskih bolesti kortizonom i adrenokortikotropnim hormonom (ACTH). Ubrzo je niz izvještaja pokazao sjajan učinak glukokortikoidne terapije za sistemski eritematozni lupus (SLE), dermatomiozitis i sistemski vaskulitis.
Danas glukokortikoidi, uprkos velikom riziku od nuspojava (uključujući i ozbiljne), ostaju kamen temeljac u patogenetskom liječenju mnogih reumatskih bolesti. Osim toga, naširoko se koriste kod mnogih hematoloških bolesti, primarnog i sekundarnog glomerulonefritisa, kao i kod brojnih gastrointestinalnih i respiratornih oboljenja, alergijskih stanja, šokova različitog porijekla i još mnogo toga. Sinteza glukokortikoida za intravensku, intramuskularnu i intraartikularnu upotrebu proširila je opseg i taktike njihove upotrebe.
Adrenalni kortikosteroidi su podeljeni u dve glavne kategorije - glukokortikoidi i mineralokortikoidi. Prvi imaju utjecaj na gotovo sve organe i sustave u tijelu, utječući na međusobne metaboličke procese, imunološke funkcije i upalne reakcije. Glavna funkcija mineralokortikoida je regulacija metabolizma vode i soli.
Raširena upotreba glukokortikoida motivirana je njihovim snažnim protuupalnim, imunosupresivnim i antialergijskim efektima.
Na 1. evropskom simpozijumu o glukokortikoidnoj terapiji preporučuje se upotreba izraza glukokortikoidi ili glukokortikosteroidi. Ostali pojmovi - „steroidi“, „kortikosteroidi“, „kortikoidi“ su preširoki ili nedovoljno tačni, pa ih nije preporučljivo koristiti.
U kliničkoj se praksi danas koriste isključivo sintetički glukokortikoidi koji imaju značajno protuupalno, imunosupresivno i antialergijsko djelovanje sa slabim ili čak nultim mineralokortikoidnim učincima, pa su prema tome među lijekovima koji se najčešće koriste u raznim oblastima medicine.
Klasifikacija glukokortikoida po hemijskoj strukturi
Prirodni (endogeni) glukokortikoidi:
* kortizol * hidrokortizon * hidrokortizon acetat
Glukokortikoidi koji sadrže sintetičko ulje:
* prednizolon * prednizon * metilprednizolon
Sintetički glukokortikoidi koji sadrže fluor:
* deksametazon * triamcinolon * betametazon
Klasifikacija glukokortikoida po trajanju delovanja
Lijekovi kratkog djelovanja (8-12 sati):
Lijekovi prosječnog trajanja djelovanja (12-36 sati):
* prednizolon * metilprednizolon * triamcinolon
Lijekovi dugog djelovanja (36-72 sati):
* parameterazon * betametazozon * deksametazon
Za depo glukokortikoide karakteristično je duže izlaganje (eliminacija u roku od nekoliko tjedana).
2.Krznoglukokortikoidni anizam
Hipotalamička-hipofiza-nadbubrežna osovina formira složen sistem koji reguliše oslobađanje glukokortikoida u fiziološkim stanjima i različitim patološkim stanjima. Proizvodnja kortizola od strane nadbubrežne kore reguliše se ACTH, izlučuje prednja hipofiza. Oslobađanje ACTH-a, zauzvrat, reguliše hormon koji oslobađa kortikotropin, čija se sekrecija kontrolira neurološkim, endokrinim i citokinim sustavom na nivou periventrikularnih jezgara hipotalamusa. Hormon koji se oslobađa od kortikotropina transportira se u malim porcijama do lokalnog portala cirkulacije hipofize, a potom do njegovog prednjeg režnja, gdje hormon oslobođen kortikotropin potiče lučenje ACTH. strana glukokortikoida
Dnevna bazna sekrecija kortizola u čovjeka iznosi oko 20 mg. Štaviše, njegovu sekreciju karakterišu fluktuacije tokom dana, s najvišim nivoima u ranim jutarnjim satima i niskim vrijednostima u večernjim satima. Najviše izlučenih kortizola (oko 90%) cirkuliše globulini u krvi koji vezuju kortikoide. Slobodni kortizol je biološki aktivni oblik hormona.
Hiperreaktivnost hipotalamo-hipofize-adrenalne ose u odsustvu upale (na primjer, kod Cushingovog sindroma) izaziva imunosupresiju i povećava osjetljivost na infekciju. Aktivacija hipotalamo-hipofize-adrenalne osi, uzrokujući porast nivoa kortizola i dovodeći do imunosupresije, može biti uzrokovana različitim stresnim faktorima, uključujući bol, emocionalnu traumu, prehladu, velike fizičke napore, infekcije, hirurške intervencije, ograničavanje ograničenja kalorija u hrani i drugo. Endogeni glukokortikoidi, uz homeostatsku ulogu, takođe modifikuju protuupalne reakcije. Dostavljaju se dokazi da oslabljen odgovor endogenih glukokortikoida igra važnu ulogu u patogenezi niza sistemskih bolesti vezivnog tkiva ili u perzistentnosti upalnog procesa. Kod reumatskih bolesti poput reumatoidnog artritisa, SLE-a, dermatomiozitisa i drugih, značajne promjene se javljaju u hipotalamičko-hipofizno-nadbubrežnoj osi, karakterizirane neodgovarajućim izlučivanjem ACTH u odnosu na cirkulirajuće citokine, neadekvatno niskim bazalnim i stimuliranim lučenjem kortizola kao odgovor na upalu, kao i značajnim smanjenjem androgen.
Primjena sintetskih glukokortikoida dovodi do inhibicije sinteze i oslobađanja i kortikotropina koji oslobađa hormon, i ACTH, i posljedično, smanjenja proizvodnje kortizola. Dugotrajna terapija glukokortikoidima rezultira atrofijom nadbubrežne žlezde i suzbijanjem hipotalamično-hipofize-adrenalne osi, uzrokujući smanjenje sposobnosti proizvodnje dodatnih endogenih glukokortikoida kao odgovor na ACTH i faktore stresa.
Trenutno je uobičajeno razlikovati dva mehanizma djelovanja glukokortikoida - genomskih i nehenomskih.
Genomski mehanizam vezanjem specifičnih citoplazmatskih receptora opažen je u bilo kojoj dozi i pojavljuje se najkasnije 30 minuta nakon formiranja hormonsko-recepcijskog kompleksa.
Temeljni mehanizam genskog djelovanja glukokortikoida je regulacija transkripcije gena koji kontroliraju sintezu proteina i DNK. Učinak glukokortikoida na glukokortikoidne receptore (koji su članovi membrane steroidnih receptora) dovodi do razvoja kompleksa događaja koji uključuju specifičnu RNK, nuklearnu RNK i druge promotorne supstance. Rezultat ove kaskade je stimulacija ili inhibicija transkripcije gena. Glukokortikoidi utječu na veliki broj gena, uključujući gene koji kontroliraju stvaranje citokina poput IL-la, IL-4, IL-6, IL-9 i gama interferona. U ovom slučaju glukokortikoidi mogu i povećati transkripciju gena i suzbiti ih.
Glukokortikoidi takođe kontroliraju sintezu ćelijskih proteina. Prolazeći lako i brzo kroz ćelijske membrane, formiraju komplekse sa steroidnim receptorima u citoplazmi koji prelaze u ćelijsko jezgro, utičući na transkripciju na genetskom aparatu
specifičnu glasnik RNA za sintezu regulatornih peptida i proteina, prvenstveno povezanih sa sistemom enzima, koji, pak, upravljaju staničnom funkcijom.Ovi enzimi mogu obavljati i stimulišuće i inhibitorne funkcije. Na primjer, oni mogu potaknuti proizvodnju proteina inhibicije u nekim ćelijama, što potpuno zaustavlja transkripciju gena u limfoidnim stanicama, čime moduliraju imunološki i upalni odgovor.
Glukokortikoidi utiču na ćelijske i humoralne imune funkcije. Razvoj limfocitopenije pod njihovim uticajem nastaje usled inhibicije proizvodnje i oslobađanja limfoidnih ćelija iz koštane srži, inhibicije njihove migracije i redistribucije limfocita u druge limfoidne sekcije. Glukokortikoidi utiču na kooperativnu interakciju T i B ćelija u imunološkom odgovoru. Oni različito djeluju na različite subpopulacije T-limfocita, uzrokujući smanjenje nivoa T-ćelija koji nose receptore za fragment IgM Fc, i bez promjene razine T-limfocita koji nose receptore za fragment IgG Fc. Pod utjecajem glukokortikoida, proliferativne sposobnosti T stanica potiskuju se i in vivo i in vitro. Učinak glukokortikoida na B-stanične odgovore očituje se u manjoj mjeri nego na T-stanicama. Dakle, kod pacijenata koji primaju srednje doze glukokortikoida opažaju se normalni odgovori antitijela na imunizaciju. Istovremeno, kratkotrajna primjena velikih doza glukokortikoida uzrokuje smanjenje nivoa IgG i IgA u serumu i ne utječe na nivo IgM. Učinak glukokortikoida na funkciju B-stanica može se posredovati zbog njihovog utjecaja na makrofage.
Za razliku od genskih, nehenomski efekti glukokortikoida rezultat su direktne fizičko-hemijske interakcije s biološkim membranama i / ili steroidno selektivnim membranskim receptorima. Negenski efekti glukokortikoida razvijaju se pod utjecajem većih doza i javljaju se nakon nekoliko sekundi ili minuta.
Negemski protuupalni učinak glukokortikoida povezan je sa stabilizacijom lizosomalnih membrana, smanjenjem propusnosti ćelijskih membrana, smanjenjem propusnosti kapilara i lokalnog protoka krvi u područjima upale, smanjenjem bubrenja endotelnih ćelija, smanjenjem sposobnosti imunih kompleksa da prodiru u bazalnu membranu, inhibiraju imunološku membranu, inhibiraju imunološku membranu, inhibiraju imunološku membranu, inhibiraju imunološku membranu, inhibiraju rast i membranu. žile u fokusu upale i smanjenje njihove propustljivosti (djelomično zbog
inhibicija sinteze prostaglandina), smanjenje broja monocita i mononuklearnih ćelija u žarištu upale, kao i učinak na polimorfonuklearne leukocite. Očito, vodeća uloga u protuupalnom učinku glukokortikoida pripada inhibiciji migracije i nakupljanju leukocita u žarištima upale. Pod utjecajem glukokortikoida dolazi do poremećaja baktericidne aktivnosti, vezivanje Fc receptora i drugih funkcija monocita i makrofaga, a nivo eozinofila, monocita i limfocita u cirkulaciji opada. Pored toga, stanični odgovori na kinine, histamin, prostaglandine i hemotaktičke faktore se mijenjaju, a oslobađanje prostaglandina iz stimuliranih stanica smanjuje. Dobro proučen nehenomski mehanizam uključuje aktiviranje endotelne sintaze dušičnog oksida.
Doza glukokortikoida određuje njihovu efikasnost, kao i učestalost i težinu nuspojava. Genski efekti glukokortikoida razvijaju se u minimalnim dozama i povećavaju se kad se dostigne približno 100 mg ekvivalenta prednizolona dnevno i ostaju stabilni u budućnosti. Ako se pri primjeni glukokortikoida u dozi do 30 mg ekvivalenta prednizolona, terapeutski rezultat gotovo u potpunosti određuje genomskim mehanizmima, tada u dozi većoj od 30 mg ekvivalenta neanomskog učinka prednizolona postaju značajni, čija se uloga brzo povećava s povećanjem doze.
Glukokortikoidi se dobro apsorbiraju u svim varijantama njihove upotrebe, tj. Za oralnu, intramuskularnu, intravensku ili intraartikularnu. Nakon oralne primjene, apsorbira se oko 50-90% glukokortikoida. Vezivanje glukokortikoida na proteine u krvi iznosi otprilike 40-90%. Metabolizam glukokortikoida izvodi se uglavnom u jetri, a izlučivanje - uglavnom putem bubrega, u obliku metabolita. Najviša koncentracija glukokortikoida u krvi nakon oralne primjene javlja se nakon 4-6 sati. Intravenskom primjenom glukokortikoida vrhunac njihove koncentracije postiže se mnogo brže. Dakle, uvođenjem 1,0 g Solomedrol® (metilprednizolon natrijum sukcinata), nakon 15 minuta primjećuje se vrhunac njegove koncentracije u plazmi. Sa intramuskularnom primjenom glukokortikoida, vrhunac njihove koncentracije u plazmi događa se značajno
kasnije. Na primjer, intramuskularnom injekcijom Depo-medrol® (metilprednizolon acetat), njegova maksimalna koncentracija u krvi postiže se nakon otprilike 7 sati.
3. Upotreba glukokortikoida
Opisani višeslojni mehanizmi djelovanja glukokortikoida i različite točke njihove primjene poslužili su kao osnova za njihovu široku upotrebu kod mnogih bolesti unutrašnjih organa, kao i niza patoloških stanja. Uz reumatske bolesti i sistemski vaskulitis, gdje su glukokortikoidi često osnovni lijekovi, koristi se i glukokortikoidna terapija u endokrinologiji, gastroenterologiji, reanimaciji, kardiologiji, pulmologiji, nefrologiji, traumatologiji i drugim.
U nastavku prikazujemo bolesti i patološka stanja u kojima se koriste glukokortikoidi:
1.Reumatoidni artritis - u nedostatku teških ekstraartikularnih manifestacija bolesti (sistemski vaskulitis, serozitis, miokarditis, fibrozirajući alveolitis, obliterani bronhiolitis), niske doze glukokortikoida koriste se na pozadini terapije koja mijenja bolest. Razvojem gore navedenih ekstraartikularnih manifestacija reumatoidnog artritisa koriste se srednje i po potrebi visoke doze glukokortikoida.
2. Ankilozirajući spondilitis - u aktivnoj fazi koriste se srednje ili visoke doze glukokortikoida.
3. Sistemski eritematozni lupus - u aktivnoj fazi bolesti kao i kada su vitalni organi i sustavi uključeni u patološki proces (teški perikarditis i / ili plevritis s ogromnim nakupljanjem eksudata i / ili miokarditisa i / ili oštećenja središnjeg živčanog sustava i / ili plućnog pneumonitisa i / ili plućna krvarenja i / ili hemolitička anemija i / ili trombocitopenična purpura i / ili aktivni lupus glomerulonefritis III, IV, V morfološka klasa) pokazuje upotrebu srednjih ili visokih doza glukokortikoida, a po potrebi i vrlo visoke FIR.
4. Akutna reumatska groznica ili pogoršanje reumatizma - srednje ili visoke doze glukokortikoida (posebno s razvojem reumatskog karditisa).
5. Reumatska polimijalgija - glukokortikoidi su lijekovi izbora. U akutnom stadijumu se koriste srednje ili visoke doze glukokortikoida.
6. Polimiozitis i dermatomiozitis - glukokortikoidi su lijekovi izbora. U akutnom stadiju propisane su visoke doze glukokortikoida.
7. Sistemska skleroderma - glukokortikoidi se propisuju u malim i srednjim dozama sa razvojem miozitisa.
8. Stillova bolest - u akutnoj fazi kao i kad su vitalni organi i sistemi (miokarditis, perikarditis, epilepsija) uključeni u patološki proces - srednje ili visoke doze glukokortikoida.
1.Giant ćelijski arteritis - u akutnom stadijumu su glukokortikoidi lijek po izboru i propisani su u velikim dozama.
2. Takayasu bolest - u akutnom stadijumu se koriste srednje ili visoke doze glukokortikoida.
3. Nodularni poliarteritis i mikroskopski poliangiitis - u akutnom stadijumu se koriste visoke doze glukokortikoida.
4. Wegenerova bolest - u akutnom stadijumu - velike doze glukokortikoida.
5. Charge-Straussov sindrom - terapija akutne faze izbora - visoke doze glukokortikoida.
6. Behcetov sindrom - u akutnoj fazi propisane su srednje ili visoke doze glukokortikoida.
7. Kožni leukocitoklastični vaskulitis - u teškim slučajevima se koriste visoke doze glukokortikoida.
8. Hemoragični vaskulitis (Shenlein-Genoch purpura) - glukokortikoidi se propisuju u srednjim ili velikim dozama s razvojem glomerulonefritisa sa nefrotskim sindromom i / ili stvaranjem 50-60% glomerula i više od pola mjeseca. Prema brojnim reumatolozima, prosječne doze glukokortikoida mogu se koristiti za abdominalni sindrom.
1.Glomerulonefritis s minimalnim promjenama (idiopatski nefrotski sindrom) - u početnim fazama bolesti ili s pogoršanjima, glukokortikoidi propisani u srednjim ili visokim dozama liječenje su izbora.
2. Fokalno-segmentalna glomeruloskleroza-hialinoza - u početnim fazama bolesti ili s pogoršanjem koristi se srednja ili velika doza glukokortikoida.
3. Mesangioproliferativni glomerulonefritis srednje ili visoke doze glukokortikoida koriste se u razvoju nefrotskog sindroma i / ili polumjeseca u 50-60% glomerula.
4. Mesangiokapilarni glomerulonefritis - velike doze glukokortikoida koriste se za razvoj nefrotskog sindroma i / ili polumjeseca u 50-60% glomerula.
5. Membranousni glomerulonefritis - u prisustvu nefrotskog sindroma koristi se srednje ili visoke doze glukokortikoida.
6. Glomerulonefritis koji brzo napreduje (subakutni, lunate) - koriste se velike doze glukokortikoida.
Sekundarni glomerulonefritis (tj. Glomerulonefritis koji se razvio sa SLE, reumatoidni artritis, polimiozitis, dermatomiozitis, vaskulitis) koriste srednje ili visoke doze glukokortikoida.
1.Nedostatak ACTH-a kod raznih bolesti hipofize - hidrokortizon ili alternativno niske doze glukokortikoida koristi se kao nadomjesna terapija.
2. Tirotoksikoza izazvana amiodaronom - koriste se velike doze glukokortikoida.
3. Nadbubrežna insuficijencija - hidrokortizon ili alternativno niske ili srednje doze glukokortikoida koriste se kao nadomjesna terapija.
1.Crohnova bolest - u akutnom stadijumu se koriste visoke doze glukokortikoida.
2. Nespecifični ulcerozni kolitis - u akutnom stadijumu se koriste srednje ili visoke doze glukokortikoida.
3. Autoimuni hepatitis - koriste se srednje ili visoke doze glukokortikoida.
4. Početni stadiji ciroze - primijenite prosječnu dozu glukokortikoida.
5. Teški alkoholni hepatitis - koriste se srednje ili visoke doze glukokortikoida.
1.Postvirusni i nespecifični limfocitni miokarditis - propisane su srednje ili visoke doze glukokortikoida.
2. Akutni ne-gnojni perikarditis sa nakupljanjem eksudata - koriste se srednje ili visoke doze glukokortikoida.
1.Bronhijalna astma - oralni glukokortikoidi (u srednjim ili visokim dozama) propisuju se za akutnu tešku astmu, teška pogoršanja astme, pri čemu inhalacioni glukokortikoidi i bronhodilatatori nisu efikasni.
2. Kriptogeni fibrozirajući alveolitis - koriste se visoke doze glukokortikoida.
3. Obliterirajući bronhiolitis - koriste se velike doze glukokortikoida.
4. Sarkoidoza pluća - koriste se srednje ili visoke doze glukokortikoida.
5. Eozinofilna pneumonija - propisane su srednje ili visoke doze glukokortikoida.
1.Hemoblastoze - koriste se visoke i vrlo visoke doze glukokortikoida.
2. Anemija (hemolitička, autoimuna, aplastična) - koriste se srednje i visoke doze glukokortikoida.
3. Trombocitopenija - propisane su srednje i visoke doze glukokortikoida.
1. Šok različitog porijekla - koristite visoke i veoma visoke doze glukokortikoida. Preporučuje se pulsna terapija.
2. Alergijske reakcije - propisane su visoke i vrlo visoke doze glukokortikoida, ako je potrebno, „pulsna terapija“.
3. Akutni respiratorni distres sindrom - koriste se vrlo visoke doze glukokortikoida.
1.Ovisno o kliničkoj situaciji, koriste se glukokortikoidi od niskih do vrlo visokih doza i, ako je potrebno, „pulsna terapija“.
4.Basic onnuspojave glukokortikoida
Kratkim tečajevima liječenja glukokortikoidima obično se ne javljaju ozbiljne nuspojave. Neki pacijenti prijavljuju porast apetita, debljanje, nervnu razdražljivost i poremećaje spavanja.
Uz produljenu primjenu kortikosteroida, takozvani Itsenko-Cushingov sindrom razvija se s teškom pretilošću, licu u obliku mjeseca, pretjeranim rastom kose na tijelu i povišenim krvnim pritiskom. Uz smanjenje doze hormona, ove su pojave reverzibilne. Najopasniji učinak glukokortikoida na sluznicu gastrointestinalnog trakta: oni mogu izazvati čireve dvanaesnika i želuca. Stoga je prisustvo pacijenta sa peptičkim ulkusom jedna od glavnih kontraindikacija upotrebi kortikoida. Kada pacijent uzima steroidne hormone, ako ima pritužbi jačine ili bolova u gornjem dijelu trbuha, žgaravice, potrebno je propisati lijekove koji smanjuju kiselost želučanog soka. Liječenje bilo kojim glukokortikoidima prati gubitak kalijuma, pa uzimanje prednizona mora biti kombinirano s uzimanjem kalijevih pripravaka (panangin, asparkum). Kortikosteroidi uzrokuju zadržavanje natrijuma i tekućine u tijelu, pa kada se pojave edemi, mogu se koristiti samo diuretici koji štede kalij (na primjer, triampur, trirezid K). Uz dugotrajno davanje kortikosteroida djeci, mogući su poremećaji rasta i odgođeni pubertet.
Svi glukokortikoidi imaju slične nuspojave, koje ovise o dozi i trajanju liječenja.
1. Suzbijanje funkcije kore nadbubrežne žlijezde. Glukokortikoidi suzbijaju funkciju hipotalamus-hipofize-nadbubrežnog sistema korteksa. Ovaj efekat može trajati mjesecima nakon prekida liječenja i ovisi o primijenjenoj dozi, učestalosti primjene i trajanju terapije. Učinak na kore nadbubrežne žlijezde može biti oslabljen ako se umjesto lijekova dugog djelovanja (dex-metazon) koriste kratkotrajni lijekovi poput prednizona ili metilprednizolona u malim dozama. Preporučljivo je uzimati cjelokupnu dnevnu dozu u ranim jutarnjim časovima, što je najviše u skladu s fiziološkim ritmom sekrecije endogenog kortizola. Kada se uzima svaki drugi dan, koriste se kratko djelujući glukokortikoidi, a propisana je i jedna doza u ranim jutarnjim časovima. Pod utjecajem stresova (trbušne operacije, teške akutne pridružene bolesti itd.) Često se javlja hipofunkcija nadbubrežne kore koja se očituje nedostatkom apetita, gubitkom težine, pospanošću, vrućicom i ortostatskom hipotenzijom. Mineralokortikoidna funkcija kore nadbubrežne žlijezde je očuvana, stoga hiperkalemija i hiponatremija, karakteristične za primarnu nadbubrežnu kortikalnu insuficijenciju, obično nisu. Pacijenti trebaju nositi posebnu narukvicu ili imati medicinsku kartu sa sobom, tako da liječnik u hitnim slučajevima zna za potrebu trenutne primjene glukokortikoida. U bolesnika koji uzimaju nekoliko tjedana više od 10 mg prednizona dnevno (ili ekvivalentna doza drugog lijeka) jedan ili drugi stupanj supresije nadbubrežne kore može potrajati i do jedne godine nakon prestanka liječenja.
2. Suzbijanje imuniteta.Glukokortikoidi smanjuju otpornost na infekcije, posebno bakterijske, rizik od infekcije ovisi o dozi glukokortikoida i ostaje glavni uzrok komplikacija i smrti pacijenata sa SLE-om. Kao rezultat liječenja steroidima lokalna infekcija može postati sistemska, latentna infekcija može postati aktivna, a mogu je izazvati i nepatogeni mikroorganizmi. Na pozadini glukokortikoidne terapije, infekcije se mogu pojaviti prikriveno, ali tjelesna temperatura obično raste. Kao preventivna mjera preporučuje se imunizacija cjepivima protiv gripe i pneumokoka, koja ne uzrokuje pogoršanje SLE-a. Prije početka liječenja glukokortikoidima, prikladno je provesti kožni tuberkulinski test.
3. Promjene u izgledu uključuju: zaokruživanje lica, debljanje, preraspodjela tjelesne masti, hirzutizam, akne, ljubičaste pruge, modrice sa minimalnim ozljedama. Ove promjene se smanjuju ili nestaju nakon smanjenja doze.
4. Mentalni poremećaji kreću se u rasponu od blage razdražljivosti, euforije i poremećaja spavanja do teške depresije ili psihoze (potonju se pogrešno može smatrati lupusnom lezijom središnjeg nervnog sistema).
5. Hiperglikemija se može pojaviti ili povećati tijekom liječenja glukokortikoidima, ali u pravilu ne služi kao kontraindikacija za njihovo imenovanje. Možda će biti potrebna upotreba inzulina, rijetko se razvija ketoacidoza.
6. Kršenja vode-elektrolitne ravnoteže uključuju zadržavanje natrijuma i hipokalemiju. Posebne poteškoće u liječenju nastaju zbog zagušenja srca i edema.
7. Glukokortikoidi mogu izazvati ili povećati arterijsku hipertenziju. I / O pulsna terapija steroidima često pogoršava postojeću arterijsku hipertenziju ako je teško lečiti.
8. Osteopenija sa kompresijskim prelomima tijela kralježaka često se razvija s produljenom terapijom glukokortikoidima. Stoga bi bolesnici trebali primiti ione kalcijuma (1-1,5 g / dnevno kroz usta). Diuretici vitamina D i tiazidi mogu biti od pomoći. U žena u postmenopauzi, pod povećanim rizikom od osteopenije, estrogeni su obično prikazani, ali rezultati njihove upotrebe u SLE-u su kontradiktorni. Kalcitoniti i difosfonati se takođe mogu koristiti. Preporučuje se vježba koja stimulira osteogenezu.
9. Steroidna miopatija karakterizira oštećenje mišića uglavnom ramenskog i karličnog pojasa. Primjećuje se mišićna slabost, ali nema bolova, aktivnosti enzima krvi mišićnog porijekla i elektromiografski parametri, za razliku od upalnog oštećenja mišića, ne mijenjaju. Biopsija mišića provodi se samo u rijetkim slučajevima kada je potrebno isključiti njihovu upalu. Mogućnost steroidne miopatije opada kako se doza glukokortikoida smanjuje i izvodi se kompleks intenzivnih fizičkih vježbi, međutim, potpuni oporavak može potrajati nekoliko mjeseci.
10. Oftalmički poremećaji uključuju porast intraokularnog pritiska (što se ponekad događa zbog napredovanja glaukoma) i posteriornu subkapsularnu kataraktu.
11. Ishemijska nekroza kostiju (aseptična, avaskularna nekroza, osteonekroza) može se javiti i tokom steroidne terapije. Te su komplikacije često višestruke, s oštećenjem glave femura i nadlahnjaka, kao i visoravni tibije. Rane abnormalnosti otkrivaju se izotopnom scintigrafijom i MRI. Pojava karakterističnih radioloških promjena ukazuje na dalekosežan proces. Hirurška dekompresija kostiju može biti efikasna u ranim fazama ishemijske nekroze, ali procjene ove metode liječenja su kontroverzne.
12. Ostale nuspojave glukokortikoida uključuju hiperlipidemiju, menstrualne nepravilnosti, pojačano znojenje, posebno noću, i benignu intrakranijalnu hipertenziju (pseudotumor cerebri). Pojava tromboflebitisa, nekrotizirajući arteritis, pankreatitis i peptički čir ponekad su povezani s djelovanjem glukokortikoida, ali dokazi o ovoj vezi nisu dovoljni.
5.Warning beatglukokortikoidi
1. Jasno obrazloženje za upotrebu glukokortikoida.
2. Obrazložen izbor glukokortikoidnih lekova, koji se karakteriše i visokom efikasnošću i relativno niskim spektrom nuspojava. Metilprednizolon (Medrol, Solu-medrol i Depo-medrol) ispunjava ove zahtjeve, argumenti za koje su dati gore.
3. Izbor početne doze glukokortikoidnog lijeka koji pruža potreban klinički učinak u njegovim minimalnim dozama trebao bi se temeljiti na dubinskoj procjeni pacijenta, uključujući nozologiju bolesti, njezinu aktivnost, prisustvo oštećenja vitalnih organa i sustava, kao i općenito prihvaćene preporuke u taktikama terapije glukokortikoida za razne kliničke situacije. Danas je terapija glukokortikoida nedvosmisleno prepoznata kao liječenje izbora za mnoge reumatske bolesti, uključujući SLE, dermatomiozitis i polimiozitis, vaskulitis, glomerulonefritis i drugo. Istovremeno se početne doze značajno razlikuju ovisno o karakteristikama kliničke slike i laboratorijskim parametrima. Tako, na primjer, s visokom aktivnošću SLE-a, dermatomiozitisom, polimiozitisom, sistemskim vaskulitisom i / ili uključenošću vitalnih organa i sistema u ove bolesti, naznačena je primjena visokih ili vrlo visokih doza glukokortikoida. Istodobno, s malom aktivnošću SLE-a, vaskulitisom, dobar klinički učinak može se postići niskim dozama glukokortikoida, a u nedostatku oštećenja unutrašnjih organa i središnjeg živčanog sustava nije potrebno propisivati glukokortikoidnu terapiju kako bi se postigla klinička remisija, jer se primjenom NSAID-a može postići dovoljan klinički učinak , obično u kombinaciji sa aminokinolinskim preparatima. Istovremeno, brojni pacijenti trebaju dodatnu upotrebu niskih doza glukokortikoida (Medrol 4-6 mg dnevno ili prednizolon 5-7.5 mg dnevno).
Raširena upotreba lijekova za modificiranje bolesti već u ranim fazama reumatoidnog artritisa, nedostatak podataka o pozitivnim učincima srednjih i visokih doza glukokortikoida na dugoročnu prognozu kod pacijenata s reumatoidnim artritisom, te visok rizik od ozbiljnih nuspojava pri njihovoj primjeni, značajno su promijenili pristup primjeni glukokortikoida. Danas u odsustvu
Ozbiljne ekstraartikularne manifestacije reumatoidnog artritisa (na primer, vaskulitis, pneumonitis) ne preporučuju se za upotrebu glukokortikoida u dozama većim od 7,5 mg dnevno prednizona ili 6 mg metilprednizolona. Štoviše, kod mnogih pacijenata s reumatoidnim artritisom, dodavanje 2-4 mg Medrola na dan na terapiju koja mijenja bolest karakterizira dobar klinički učinak.
1. Uspostavite tehniku uzimanja glukokortikoida: neprekidne (dnevne) ili isprekidane (alternativne i isprekidane) opcije.
2. Kod većine reumatskih bolesti vaskulitis, glomerulonefritis, glukokortikoidi obično nisu dovoljni za postizanje potpune ili djelomične kliničke i laboratorijske remisije, što zahtijeva njihovu kombinaciju s različitim citotoksičnim lijekovima (azatioprin, ciklofosfamid, metotreksat i drugi). Uz to, primjena citostatika može značajno smanjiti dozu glukokortikoida (ili ih čak ukinuti) uz zadržavanje dobivenog kliničkog efekta, što značajno smanjuje učestalost i ozbiljnost nuspojava terapije glukokortikoidima.
3. Mnogi kliničari preporučuju da se kod mnogih pacijenata s reumatskim bolestima nakon postizanja kliničke i laboratorijske remisije nastavi dugotrajno vrlo nisko doziranje glukokortikoida (2-4 mg / dan Medrol® ili 2,5-5,0 mg / dan prednizolona).
Sapopis korištene literature
1 predavanje Dr. Prof. Lobanova E.G., Ph.D. Chekalina N.D.