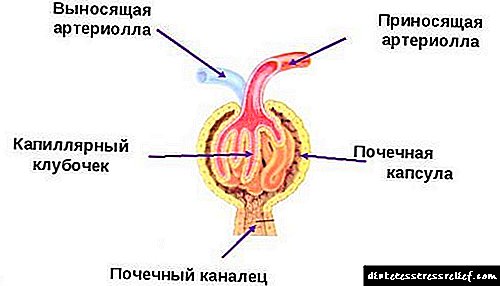
Terapijski arhiv broj 03 2018 - Hemohromatoza - trenutno stanje problema

Hemokromatoza je nasljedna patologija povezana s velikom apsorpcijom željeza u organima probave i njegovim naknadnim prekomjernim nakupljanjem u raznim unutrašnjim organima.
Jetra pati više od ostalih. Rano otkrivanje hemokromatoze, njegova dijagnoza i liječenje neće dopustiti razvoj posljedica.
Hemohromatoza - savremeno stanje problema
N.B. VOLOSHINA1, M.F. OSIPENKO1, N.V. LITVINOVA1, A.N.VOLOSHIN2
1 Novosibirski državni medicinski univerzitet FGBOU u NSMU Ministarstva zdravlja Rusije, Rusija,
2Novosibirska gradska klinička bolnica 2, Rusija
Sindrom preopterećenja željezom može biti povezan sa različitim stečenim stanjima i nasljednim faktorima. Nasljedna hemokromatoza je najčešći genetski poremećaj. Bez terapijske intervencije bolest može dovesti do razvoja opasnih po život komplikacija kao što su ciroza, hepatocelularni karcinom. U članku su predstavljeni podaci o patogenezi, dijagnozi i liječenju nasljedne hemokromatoze. Daju se vlastita klinička zapažanja.
Ključne riječi: nasljedna hemokromatoza, liječenje, flebotomija.
 Hemohromatoza je bolest povezana sa nakupljanjem visokog patološkog nivoa željeza u tijelu, što dovodi do funkcionalnih poremećaja nekih organa. Tipično je apsorpcija željeza usko regulirana, što rezultira time da tijelo nije u stanju izlučiti višak željeza. Višak željeza akumulira se u ćelijama kao hemosiderin. To na kraju dovodi do ćelijske smrti i zamjene ovih ćelija vlaknastim tkivom, što dovodi do poremećaja strukture i funkcije organa. Uz hemokromatozu moguće je oštećenje jetre, gušterače, srca, štitne žlijezde, zglobova, kože, žlijezda i hipofize.
Hemohromatoza je bolest povezana sa nakupljanjem visokog patološkog nivoa željeza u tijelu, što dovodi do funkcionalnih poremećaja nekih organa. Tipično je apsorpcija željeza usko regulirana, što rezultira time da tijelo nije u stanju izlučiti višak željeza. Višak željeza akumulira se u ćelijama kao hemosiderin. To na kraju dovodi do ćelijske smrti i zamjene ovih ćelija vlaknastim tkivom, što dovodi do poremećaja strukture i funkcije organa. Uz hemokromatozu moguće je oštećenje jetre, gušterače, srca, štitne žlijezde, zglobova, kože, žlijezda i hipofize.
Preopterećenje željezom, koje uzrokuje hemokromatozu, može se dogoditi na tri načina: masivan oralni unos željeza, povećana apsorpcija željeza tijekom normalnog unosa željeza i prekomjerna proizvodnja ili masivna, česta transfuzija crvenih krvnih zrnaca.
Kod nasljedne hemokromatoze višak željeza se obično odlaže u parenhimskim ćelijama, dok se kod transfuzijske hemokromatoze uglavnom taloži u retikuloendotelnim ćelijama 1-3.
Nasljedna hemokromatoza uključuje skupinu genetskih poremećaja koja je karakterizirana povećanom apsorpcijom željeza. Prevladavajući mehanizam u većini vrsta nasledne hemokromatoze je efekt hepcidina, koji igra ključnu ulogu u homeostazi gvožđa 4–6. Hepsidin se sintetizira uglavnom u hepatocitima i kontrolira koncentraciju željeza u plazmi vezanjem na feroportin (koji se također naziva SLC40A1), jedini poznati transmembranski transporter željeza iz tkiva donatora željeza. Feroportin izvozi gvožđe iz dvanaesnika, iz makrofaga i hepatocita.
U plazmi se željezo veže na trasferrin, pa je zasićenost željezom transferinom u prosjeku 35% (prosječna jutarnja vrijednost). Hepsidin inhibira oslobađanje željeza iz makrofaga (iz starih crvenih krvnih zrnaca i feritina), hepatocita i enterocita dvanaestopalačnog creva vezanjem na feroportin. I u nedostatku feroportina, blokiran je izlaz željeza iz enterocita, hepatocita i makrofaga. Tako hepcidin smanjuje apsorpciju željeza u crijevima, smanjuje nivo oslobođenog željeza iz hepatocita i makrofaga, što dovodi do niskog nivoa željeza u plazmi i povećanja tkiva.
Uzrok nasljedne hemokromatoze je mutacija u HFE genu. Poraz gena HFE prvi je put opisan 1996. godine, što je mutacija koja dovodi do zamjene tirozina cisteinom na položaju aminokiseline 282 (C282Y). Mutacija u HFE genu uzrokuje pojačanu apsorpciju željeza i pored normalnog unosa željeza. HFE protein reguliše proizvodnju hepcidina. Pacijenti sa nasljednim homozigotama hemokromatoze C282Y su od 80 do 85% 1, 8.
Postoje još dvije mutacije: jedna je povezana sa zamjenom aspartata histidinom na položaju 63 (H63D), a druga je zamjena cisteina serinom u položaju 65 (S65C). Ove mutacije nisu povezane sa sindromom preopterećenja željezom, osim ako je C282Y sastavni dio heteroziga C282Y / H63D ili C282Y / S65C. Dakle, nasljedna hemokromatoza povezana sa HFE može se potvrditi asimptomatskim tokom bolesti. U skladu s tim, genetska dijagnoza može se primijeniti kod pacijenata kod kojih se hemokromatoza još nije fenotipično očitovala. Ova grupa bolesnika sa genetskom predispozicijom za hemohromatozu. Heterozigoti imaju povećan rizik od razvoja dijabetesa u poređenju s općom populacijom, mehanizam razvoja nije poznat 9–11.
Ranije se mislilo da će se kod svih bolesnika s oštećenjem gena HFE s vremenom razviti klinika za hemokromatozu. Međutim, sada je utvrđeno da se fenotipska ekspresija nalazi samo u otprilike 70% homozigota C282Y, a manje od 10% njih razvija ozbiljno preopterećenje željezom s oštećenjem unutrašnjih organa 12, 13.
Tablica prikazuje klasifikaciju sindroma preopterećenja željeza ovisno o uzroku njegove pojave.
Ovisno o uzroku bolesti, bolesnici sa sindromom preopterećenja željezom mogu se podijeliti u 4 skupine: bolesnici sa nasljednom hemokromatozom, pacijenti s sekundarnom hemokromatozom uzrokovanom različitim uzrocima i mala skupina bolesnika, koji se ističe kao "različiti".
Uzrok sekundarne hemokromatoze je eritropoetička hemokromatoza. Najčešće se to događa kao posljedica bolesti krvi u kojoj crvena krvna zrnca imaju kraći životni vijek. U ovu grupu bolesti spadaju anemija nedostatka gvožđa, talasemija, sideroblastična anemija, hronična hemolitička anemija, aplastična anemija, anemija osjetljiva na piridoksin, manjak piruvat kinaze.
Sindrom preopterećenja željezom može se pojaviti kod pacijenata koji primaju dugotrajne i višestruke transfuzije crvenih krvnih zrnaca. Kao što se može vidjeti iz tablice, druge prilično rijetke bolesti, poput na primjer porfirije, također mogu izazvati sindrom preopterećenja željezom.
Najzad, prekomerni unos gvožđa može izazvati hemokromatozu. Dobro poznata povijesna činjenica: upotreba piva napravljenog u čeličnim bubnjevima bila je uzrok sindroma preopterećenja željezom. Također, predoziranje željeznim pripravcima može uzrokovati sindrom preopterećenja željezom. Mora se imati na umu da mnogi dodaci bez recepta sadrže željezo u dovoljno velikoj dozi, tako da je njihova nekontrolisana upotreba neprihvatljiva.
Simptomi bolesti ovise o organu koji je najviše pogođen, međutim, gotovo svi pacijenti žale se na značajnu slabost i umor. Nema specifičnih simptoma hemokromatoze. Najčešće se dijagnoza postavlja u fazi bolesti, kada je već pogođeno nekoliko sistema. Od prvih simptoma bolesti do provjere dijagnoze obično traje najmanje deset godina. Kod žena sa hemokromatozom simptomi bolesti se manifestuju u kasnijoj dobi nego kod muškaraca, zbog menstrualnog gubitka krvi, gubitka „majčinog željeza“ tokom trudnoće i antioksidacijskog djelovanja estrogena, a bolest se klinički ne očituje prije klimakterijskog perioda.
Otprilike 50% bolesnika sa simptomima nasljedne hemokromatoze ima dijabetes melitus, rizik od njegove pojave značajno se povećava kod heterozigota. Ciroza jetre prisutna je kod 70% pacijenata sa hemohromatozom. U ovoj skupini bolesnika izrazito je povećana učestalost hepatocelularnog karcinoma koji je vodeći uzrok smrti.
Oštećenje zglobova hemokromatozom manifestuje se u obliku artralgije (obično drugog i trećeg metakarpofazalnog zgloba). Deformacije zglobova s hemokromatozom obično se ne javljaju, iako su moguće i degenerativne promjene u zglobovima. Kod ovih pacijenata u pravilu se u sinovijalnoj tečnosti nalaze kristali kalcijumovog pirofosfata. Karakteristično je za poliartritis s hemokromatozom da i nakon normalizacije zaliha željeza i dalje može napredovati.
Taloženje željeza u vlaknima srčanog mišića i stanicama provodnog sistema srca može dovesti do poremećaja srčanog ritma i / ili dilatacijske kardiomiopatije, s daljnjim razvojem zatajenja srca. U nekim slučajevima postoji potpuna kompenzacija zatajenja lijeve komore nakon što se normalizira nivo željeza u tijelu 9-12.
Uz hemokromatozu moguć je razvoj hipogonadizma i, shodno tome, impotencije uslijed hipotalamičke i / ili hipofizne insuficijencije, što dovodi do kršenja oslobađanja hormona gonadotropina. U slučaju viška zaliha željeza pet puta ili više, dolazi do hiperpigmentacije kože koja je rezultat taloženja željeza i melanina. Preopterećenje željezom makrofazima može dovesti do oslabljene fagocitoze i smanjenog imuniteta, što dovodi do povećanog rizika od infekcije Listeria, Yersinia enterocolitica i Vibrio vulnificus. Taloženje gvožđa u štitnoj žlezdi obično uzrokuje hipotireozu.
Razvijeni stadij hemokromatoze karakterizira prisutnost ciroze, dijabetesa melitusa i pigmentacije kože (tzv. Bronzani dijabetes). U bolesnika koji zloupotrebljavaju alkohol i zaraženi su hepatitisom B i / ili C, patologija jetre i gušterače povezana sa hemokromatozom prolazi znatno teže 1-3.
Dijagram prikazuje dijagnostičke mjere za sumnju na hemokromatozu. Poznato je da samo oko 70% C282Y homozigota ima povišenu razinu feritina, što odgovara povećanju zaliha željeza, a samo mali procenat tih pacijenata ima kliničke manifestacije bolesti. Naravno, svi pacijenti sa simptomima koji se mogu javiti hemokromatozom trebaju biti podvrgnuti daljnjem ispitivanju kako bi se isključila bolest. Posebnu pažnju treba obratiti pacijentima sa nemotiviranom slabošću, artralgijom, bolom u gornjem desnom kvadrantu trbuha, impotencijom, smanjenim libidom, sindromom zatajenja srca, pigmentacijom kože i dijabetesom. Uz to, kod svih bolesnika sa hepatomegalijom, citolitičkim sindromom, s cirotičnim stadijom bolesti, potrebno je pored svih mogućih etioloških uzroka bolesti zapamtiti i mogućnost hemokromatoze. Naravno, nasljednu hemokromatozu treba isključiti kod pacijenata s rođacima prvog stepena srodstva koji pate od hemokromatoze. 
Ispitivanje treba započeti mjerenjem zasićenosti serumskog transferrina ili koncentracije feritina u serumu. Treba napomenuti da određivanje transferrina u slučajevima eritropoetičke hemokromatoze nije tako učinkovito za provjeru sindroma preopterećenja željezom. Specifičnost feritina u velikoj mjeri ovisi o prisutnosti upalnih bolesti. Ako je nivo feritina viši od 200 µg / l kod žena ili 300 µg / l kod muškaraca ili je zasićenost transferrinom veća od 40% kod žena ili 50% u muškaraca, potrebno je daljnje ispitivanje kako bi se isključila hemokromatoza 1, 2, 10, 11.
Prema preporukama Američkog udruženja za proučavanje bolesti jetre 2011 (AASLD 2011) ako pacijent ima transferrin u serumu od 1000 mg / l), a ovisno o tim pokazateljima, donosi se odluka o terapijskoj taktizi i potrebi biopsije jetre (vidjeti tablicu )
U bolesnika koji imaju kombinaciju heterozigota C288Y / H63D, kao i C288Y heterozigota ili ne C288Y, potrebno je pažljivo uklanjanje drugih bolesti jetre ili krvi (ako je potrebno, potrebna je punkcija biopsije jetre) i tada se donosi odluka o terapijskom krvotoku.
Ne postoje pouzdani dokazi da određena dijeta utječe na nastanak ili napredovanje hemokromatoze. Međutim, neki autori smatraju da je bolesnicima sa nasljednom hemokromatozom prikazana dijeta s izuzetkom čaja i agruma, koji, prema njihovom mišljenju, doprinose nakupljanju gvožđa. Naravno, alkohol koji je glavna hepatotoksična supstanca treba strogo zabraniti pacijentima koji imaju hemokromatozu. Pored toga, dokazano je da etanol smanjuje sintezu hepcidina 20, 21.
Primarni tretman za primarnu hemokromatozu je krvotok. Smanjenje broja crvenih krvnih zrnaca, koji su glavni mobilizator željeza u tijelu, i na taj način smanjuje i minimizira toksični učinak željeza. Pacijentima će možda trebati 50-100 krvnih zrnaca godišnje, po 500 ml, kako bi snizili nivo željeza na normalne vrednosti. Jednom kada se razina željeza normalizira, potrebno je doživotno, ali rjeđe prokrvljevanje krvi, obično 3-4 puta godišnje. Cilj krvotoka je održavanje nivoa feritina od 50–100 µg / L. U slučajevima značajnog smanjenja hemoglobina nakon nakupljanja krvi, preporučuje se zajedničko liječenje eritropoetinom.
Ako se hemokromatoza otkrije u ranoj fazi bolesti, liječenje krvotok može spriječiti disfunkciju pogođenih organa i time povećati životni vijek pacijenta. Međutim, pacijenti rijetko žive više od dvije godine nakon dijagnoze, u slučajevima kasne dijagnoze u fazi detaljnih kliničkih manifestacija 22, 23.
Prema Europskom udruženju za proučavanje jetre (EASL 2010), indikacije za terapijsko prokrvljenost krvi su povišeni nivoi feritina u serumu. Preporučuje se terapijsko propisivanje krvi s volumenom od 400-500 ml jednom tjedno ili jednom svaka 2 tjedna dok se ne dosegne razina feritina od 45% i značajnog povećanja feritina u serumu do 1444 mcg / l, dijagnoza hemokromatoze nije moguća. DNK uzorci analizirani su na mutacije HFE gena - pronađena je mutacija C282Y (c.845 G> A) u homozigotnom stanju s.845A / s.845 A.
Dakle, dijagnoza bolesnika K. je nasljedna hemokromatoza, homozigotna mutacija u HFE genu (C288Y / C288Y) s pretežnim oštećenjem jetre, fibroza 1. stupnja (FibroScan, Metavir 6,6 kPa).
Kasna manifestacija i dijagnoza bolesti u 58. godini života u 2015. godini nastaje zbog dugoročne nadoknade bolesti uslijed masovnog gubitka krvi zbog menstrualne krvi, davanja krvi i gubitka krvi tijekom prekida trudnoće i porođaja.
Zanimljivo je da je od prvih znakova bolesti do provjere dijagnoze prošlo 8 godina! Od kraja 2015. pacijentu je propisana terapija - isticanje krvi od 500 ml jednom nedeljno. Pacijent je dobro podnio krvotok, primijetio značajno poboljšanje stanja nakon prvog postupka. Praćen je opći test krvi i feritin u krvi, čija se razina postupno smanjivala. Ukupno je obavljeno više od 100 krvožilnih krvi u 2 godine, međutim, do danas, ciljna razina transferina (100 µg / l) nije postignuta zbog toga što pacijentica periodično preskače postupak, objašnjavajući svoje dobro zdravlje. Trenutno pacijentkinja nastavlja terapiju, uspjela ju je uvjeriti u potrebu doživotne terapije.
Stoga se mora zapamtiti da u prisutnosti citolitičkog sindroma u bolesnika treba uključiti nasljednu hemokromatozu u dijagnostičku pretragu. Terapija izbora za nasljednu hemokromatozu trenutno ostaje krvopija. Adekvatna terapija započeta na vrijeme omogućava izbjegavanje razvoja cirotičnog stadija bolesti i time povećava životni vijek pacijenata.
Podaci o autorima:
Vološina Natalija Borisovna - kandidat medicinskih nauka, vanredni profesor propaedeutika unutrašnjih bolesti medicinskog fakulteta
Osipenko Marina Fedorovna - doktor medicinskih nauka, prof., vod. kafe propaedeutika unutrašnjih bolesti medicinskog fakulteta
Voloshin Andrey Nikolaevich - Ljekar Novosibirske gradske kliničke bolnice 2
Hemohromatoza: šta je ova bolest?
Da biste shvatili suštinu bolesti, morate znati koliko željeza čovjek treba normalno da posjeduje. U muškaraca je željezo oko 500-1500 mg, a u žena od 300 do 1000 mg. Pokazatelji ne ovise samo o spolu, već i o težini osobe. Više od polovine ukupne količine gvožđa nalazi se u hemoglobinu.
Oko 20 mg ovog mikroelementa ulazi u organizam s hranom dnevno. Od toga se samo 1-1,5 mg apsorbira u crijeva. Sa hemohromatozom (GC) ili siderofilijom, kako se ova bolest naziva, apsorpcija se povećava na 4 mg dnevno, a željezo se postepeno nakuplja u tkivima različitih organa.
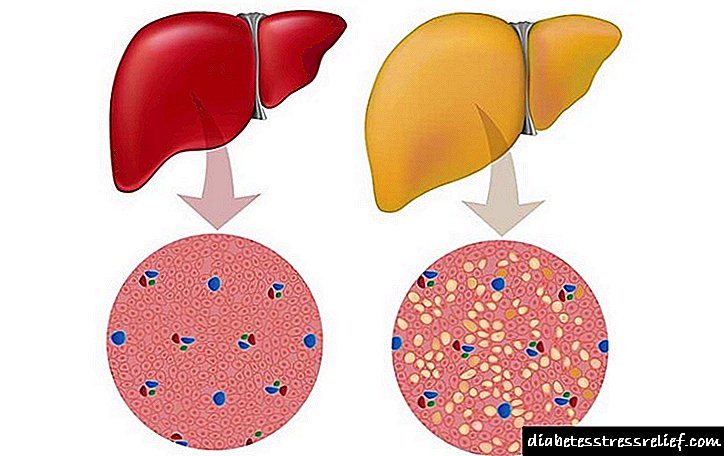
Zdrava jetra i hemohromatoza
Njegov višak uništava molekule proteina i ugljikohidrata, a samim tim i organ. U bolesnika sa GC-om količina željeza u jetri može doseći 1% suhe mase organa što je upareno s cirozom, a u trećini slučajeva s rakom jetre. Oštećen viškom željeza, gušterača može dati podsticaj razvoju dijabetesa.
Odloženo u hipofizi gvožđe uništava čitav endokrini sistem. Reproduktivni organi pate više od ostalih: muškarci imaju erektilnu disfunkciju, a žene mogu razviti neplodnost.
Uzroci
Glavni razlog GC je "neispravnost" gena, tačnije HFE gena. On je taj koji reguliše tok hemijskih procesa i količinu gvožđa koji ulazi u organizam kao dio hrane. Mutacija koja se u njemu događa vodi do poremećaja metabolizma željeza.
Ostali uzroci GC-a su:
- talasemija U tom se slučaju struktura hemoglobina uništava ispuštanjem željeza,
- hepatitis
- gvožđe se može povećati kao rezultat čestih transfuzija krvi. Činjenica je da je životni vijek vanzemaljskih crvenih krvnih zrnaca znatno kraći od njihovog vlastitog. Kada umru, oni oslobađaju željezo,
- postupci hemodijalize.
ICD-10 kod i klasifikacija
U općenito prihvaćenom klasifikatoru GC bolesti dodjeljuje se kod E83.1.
U etičkoj veni razlikuju se primarni (ili nasljedni GC) i sekundarni:
- primarna. Ova vrsta bolesti ima nasljednu prirodu i rezultat je oštećenja enzimskog sistema koji utječe na metabolizam željeza. Dijagnosticira se kod 3 osobe od 1000. Napominje se da su muškarci podložniji ovoj patologiji i da pate od nje 3 puta češće od žena,
- sekundarno. Njegov uzrok su oboljenja jetre pacijenta (koja se često primjećuje kod alkoholizma), transfuzija krvi, samo liječenje vitaminskim kompleksima s visokim udjelom željeza. Uzrok stečenog GC-a mogu biti kožni problemi i krvne bolesti.
Primarna hemokromatoza (PCH) karakterizira postepeni razvoj, a u ranoj se fazi pacijenti žale na umor. Možda ih muči bol u desnoj strani i suha koža.
Prošireni stadij PCH karakterizira:
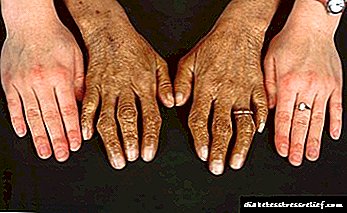
- specifična pigmentacija lica, vrata, ruku i pazuha. Poprimaju brončani nijansu,
- ciroza jetre. Dijagnosticira se u 95% slučajeva,
- zatajenje srca
- artritis
- dijabetes melitus: u 50% slučajeva
- uvećana slezina,
- seksualna disfunkcija.
U posljednjim fazama uočava se portalna hipertenzija i ascites. Može se razviti karcinom jetre.
 Budući da se višak željeza stvara tijekom godina, početni simptomi sekundarnog GC-a manifestuju se kod muškaraca nakon 40. godine, a kod žena nakon 60. godine.
Budući da se višak željeza stvara tijekom godina, početni simptomi sekundarnog GC-a manifestuju se kod muškaraca nakon 40. godine, a kod žena nakon 60. godine.
Simptomi su sljedeći:
- melasma,
- umor i gubitak težine,
- smanjen libido
- povećanje i zgušnjavanje jetrenog tkiva,
- ciroza (u zadnjem stadiju GC).
Krvni test i druge dijagnostičke metode
 Gastroenterolog potvrđuje dijagnozu. U ranim fazama bolesti laboratorijski testovi su vrlo važni.
Gastroenterolog potvrđuje dijagnozu. U ranim fazama bolesti laboratorijski testovi su vrlo važni.
Uz GC, vrše se posebni testovi krvi kako bi se otkrile vrijednosti željeza u plazmi, njegova niska sposobnost vezanja gvožđa i zasićenost transferinom.
Glavni simptom bolesti su naslage hemosiderina u hepatocitima jetre, kože i ostalih organa koji postaju „zahrđali“ zbog viška ovog pigmenta. Za biohemiju je potrebna i opšta proba krvi, kao i šećer. Osim toga, uzimaju se jetreni testovi.
 Pored toga, izvode se i instrumentalne studije:
Pored toga, izvode se i instrumentalne studije:
- biopsija jetre je glavni način da se potvrdi GC,
- Ultrazvuk abdomena
- MRI jetre (u nekim slučajevima)
- ehokardiografija, kako bi se isključila / potvrdila kardiomiopatija,
- zajednička radiografija.
Terapijska dijeta
Važno je razumjeti da s dijagnosticiranom hemohromatozom dijeta treba biti doživotna.
Glavno pravilo je maksimalno smanjenje ishrane proizvoda koji sadrže željezo, posebno:

- tvrdi sirevi i morska riba,
- žitarice: zob, proso i heljda,
- crni hljeb
- mahunarke i suho voće,
- askorbinska kiselina i lijekovi s visokim sadržajem vitamina C,
- katranica, posebno jetra, potpuno je isključena.
Alkohol je apsolutni tabu. No, čaj i kafa su prikazani naprotiv. Imaju tanin koji usporava apsorpciju željeza.
Lista korištenih lijekova
Ovaj tretman se izvodi lijekovima koji uklanjaju željezo iz tijela pacijenta. U početnoj fazi propisani su vitamini A, E i folna kiselina. Tada se koriste helatori (poput Desferal-a).

Doziranje ubrizgavanja: 1g / dan. Već 500 mg lijeka daje opipljiv rezultat: izlučuje se do 43 mg željeza. Kurs traje do 1,5 mjeseci. Duga upotreba je opasna: moguće je zamagljivanje objektiva.
Flebotomija i drugi terapijski postupci
 Flebotomija je najjednostavniji i istovremeno prilično efikasan nefarmakološki tretman GC-a.
Flebotomija je najjednostavniji i istovremeno prilično efikasan nefarmakološki tretman GC-a.
U pacijentovoj veni se vrši punkcija, a krv izlazi iz tela. Tjedno se ispije oko 500 ml.
Procedura je samo ambulantna. Krv se neprestano testira na koncentraciju ferina: trebala bi pasti na 50. To može potrajati 2-3 godine. Nadalje, terapija je usmjerena na održavanje optimalne vrijednosti ovog elementa u tragovima.
Liječenje narodnim lijekovima
Ova terapija ima blagi učinak na oboljele organe.
Liječenje jetre:

- bundeva. Dobar je i sirov i pečen. Povrće se dodaje salatama ili miješa sa medom - ukusno i zdravo! Takođe je prikazan sok od bundeve: pola čaše na prazan stomak,
- cvekla- Još jedan koristan proizvod za GC. Koristite u sirovom ili kuvanom obliku. Zdravi i svježe cijeđeni sok.
Za liječenje srca možete savjetovati infuzije gloga, adonisa ili matičnjaka. Biljke se prelijeju kipućom vodom i, nakon insistiranja, piju se prema uputstvu.
Liječenje gušterače:

- Dekocija sjemenki plantaže pomoći će. Proporcije: 1 tbsp. sirovine na 1 tbsp. voda. Zakuhano sjeme se kuha 5 minuta, hladi i uzima se prije jela, 1 kašika,
- med sa cimetom. Proporcije: 1 tbsp. praha na 1 kašiku vode. Inzistirajte na 15-30 minuta. i dodajte malo meda. Ostaviti još 2 sata. Sva sredstva treba piti u toku dana.
Korisna i nekuhana kaša (sa ljuskom). Proporcije: 100 g žitarica na 1,5 litara vode. Kuhajte najmanje pola sata. Zatim, pravo u zdjelu u kojoj se kuhao zob, zdrobite ga do grila i kuhajte ponovo 40 minuta. Život filtriranog bujona ne može biti više od 2 dana. Popijte pola čaše prije jela.
Prognoza i glavne kliničke smjernice
Ali ako se terapija izvodi pod medicinskim nadzorom i na vreme, tada se život pacijenta znatno povećava.
Budući da je nasljedna bolest, hemokromatoza se u 25% slučajeva dijagnosticira kod rodbine pacijenta. Oni se moraju dalje ispitati. To će otkriti bolest i prije kliničkih manifestacija te u budućnosti izbjeći njene komplikacije.
U slučaju sekundarnog GC-a preporučuje se ishrana, važno je držati jetru i krv pod kontrolom. Hemokromatoza otkrivena tokom trudnoće (ili u fazi planiranja) nije opasna.
Srodni videozapisi
O simptomima, uzrocima i načinima liječenja hemohromatoze u videu:
Nažalost, još uvijek nije utvrđen osnovni uzrok hemokromatoze. Ali trenutno je razvijena i aktivno se koristi posebna sveobuhvatna tehnika liječenja, čija je svrha prekinuti kliničke manifestacije bolesti i smanjiti rizik od mogućih komplikacija.
- Dugotrajno stabilizuje nivo šećera
- Obnavlja proizvodnju inzulina pankreasa
Saznajte više. Nije droga. ->
Istodobna terapija bolesti
Prekomjerno željezo u organima dovodi do razvoja više patologija. Svi oni zahtijevaju adjuvantnu terapiju. Na primjer, ako je GC doprinio razvoju dijabetesa, posljednji se mora liječiti, uvijek držeći kontrolu šećera.
Ako se otkriju patologije u jetri, njeno liječenje je u toku. Ovo je potrebno kako bi se spriječio razvoj patologije u stanje malignog tumora.
Hemohromatoza
Nasljedna hemokromatoza (NG) je polisistemska bolest koja se temelji na genetski utvrđenim metaboličkim poremećajima željeza, što dovodi do njegovog prekomjernog nakupljanja u tijelu i toksičnog oštećenja organa i tkiva.
Prvi opis bolesti pripada A. Trousseau (1865), koji je identificirao trijadu glavnih kliničkih manifestacija: dijabetes melitus, bronzana pigmentacija kože, ciroza. Izraz "hemokromatoza" predložio je 1889. godine F.D. von Recklinghausen Od 1935. godine bolest pripada grupi nasljednih bolesti. 1996. J.N. Feder i dr. identificirao gen za nasljednu hemokromatozu (HFE), čija mutacija najčešće dovodi do razvoja ove bolesti. U 2000-2004 opisane su mutacije drugih gena koji dovode do razvoja hemokromatoze.
Prevalencija bolesti varira od 1: 250 pojedinaca koji žive u sjevernoj Europi do 1: 3300 među crnom populacijom SAD-a i afričkih zemalja. Bolest se dijagnosticira kod muškaraca 5-10 puta češće nego kod žena. Tijekom genetičkog skrininga ustanovljeno je da je homozigotna mutacija gena HFE otkrivena u 1 od 500 pregledanih pacijenata, dok je broj klinički utvrđenih slučajeva NG-a 1: 5.000. Dakle, značajan broj slučajeva bolesti nije prepoznat ili dijagnosticiran kasno, u fazi nepovratnih unutarnjih oštećenja. organa (ciroza, dijabetes melitus, dilataciona kardiomiopatija).
U skladu s genetskom osnovom bolesti razlikuju se 4 vrste nasljedne hemokromatoze:
Tip I - nasljeđuje se autozomno recesivnim mehanizmom, zbog mutacija HFE gena smještenog na hromozomu 6. Najčešće (kod 87-90% pacijenata) bilježi se mutacija C282Y - zamjena cisteina tirozinom u 282. aminokiselini. Mutacija H63D rjeđa je - zamjena citidina ganinom u 63. aminokiselini,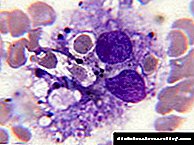
Tip II - juvenilna hemokromatoza je retka, usled mutacija u genu odgovornog za sintezu drugog proteina metabolizma gvožđa - hepsidina,
Tip III - genetska osnova sastoji se od mutacija gena koji kodira sintezu receptora transferrina,
Tip IV - genetska osnova sastoji se od mutacija gena SLC40A1, koji kodira sintezu transportnog proteina feroportina.
Etiologija i patogeneza
Željezo je s jedne strane neophodna biokemijska komponenta najvažnijih metaboličkih procesa i s druge strane je potencijalno toksičan element koji može uzrokovati oksidativna oštećenja bioloških membrana, proteina i nukleinskih kiselina. U skladu s tim, homeostaza gvožđa u ljudskom tijelu je strogo regulirana. Većina ovog elementa prolazi postupak recikliranja: makrofagi slezine i jetre hvataju i uništavaju staračka crvena krvna zrnca, razgrađuju hemoglobin i oslobađaju željezo, koje se veže na transferrin ili feritin i reciklira se. Dnevni fiziološki gubitak željeza ne prelazi 1-2 mg i nadoknađuje se apsorpcijom ekvivalentne količine željeza u gastrointestinalnom traktu. Ne postoje mehanizmi koji kontrolišu eliminaciju željeza u ljudi.
Mutacije gena odgovornih za sintezu proteina uključenih u metabolizam željeza dovode do neravnoteže između unosa i gubitka željeza, patološkog nakupljanja ovog elementa u organima i tkivima i do pojave slobodnog (nije povezano s transferrinom) željeza u krvi. Razvoj hemokromatoze tipa I povezan je s mutacijom gena odgovornog za sintezu HFE proteina (hemokromatozni protein), koji je glikoprotein (MM = 37,235 daltona), po strukturi sličan proteinima glavnog kompleksa histokompatibilnosti klase 1. Funkcija HFE proteina u metabolizmu željeza i mehanizam naglog povećanja apsorpcije željeza tijekom mutacija u HFE genu nisu u potpunosti utvrđeni.
Patogeneza hemokromatoze tipa II-IV povezana je s mutacijama gena koji kodiraju druge proteine koji sudjeluju u metabolizmu željeza - hepsidin, receptor za transferrin-II, feroportin.
Izrazita karakteristika NG tipa IV, koja se temelji na mutacijama gena feroportina, prevladava kršenje procesa recikliranja željeza, što se fenotipično manifestuje kao duboka hipohromna anemija i eritropoeza nedostatka željeza u kombinaciji sa teškom hemokromatozom unutrašnjih organa.
Patološka nakupljanja željeza u parenhimskim organima povezana su s degenerativnim promjenama ćelijskog parenhima i progresivnim razvojem vlaknastog tkiva što dovodi do nepovratne disfunkcije vitalnih organa. Najugroženiji ciljni organi su jetra, srce i gušterača.
Klinički znaci i simptomi
Klinička slika NG određena je nivoom nakupljanja gvožđa u organima i tkivima. Kod hipertenzije tipa I kliničke manifestacije se obično nalaze u dobi od 45-50 godina i starije. Kod maloljetničke hemokromatoze (tip II) jake lezije jetre i srca pojavljuju se rano - u drugoj ili trećoj dekadi života. U muškaraca se kliničke manifestacije bolesti opažaju 3 puta češće nego kod žena što je povezano s fiziološkim karakteristikama ženskog tijela. Glavne kliničke manifestacije uključuju simptome oštećenja jetre, srca, organa endokrinog sistema i zglobova.
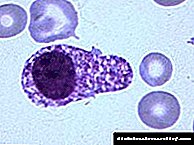 Znakovi oštećenja jetre mogu se otkriti tijekom nasumičnog pregleda u obliku nemotiviranog porasta transaminaza ili debu sa simptomima portalne hipertenzije: ascitesom, hepatosplenomegalijom, krvarenjem iz varikoznih vena jednjaka i želuca.
Znakovi oštećenja jetre mogu se otkriti tijekom nasumičnog pregleda u obliku nemotiviranog porasta transaminaza ili debu sa simptomima portalne hipertenzije: ascitesom, hepatosplenomegalijom, krvarenjem iz varikoznih vena jednjaka i želuca.
Simptomi oštećenja srca uključuju srčani udar, razvoj aritmija i znakove zatajenja srca. Teška kardiomiopatija je vodeći uzrok smrti u mladih pacijenata.
Razvoj dijabetesa i disfunkcija genitalnih žlijezda karakteristični su simptomi NG-a. Kod muškaraca se često primjećuje atrofija testisa, smanjen seksualni nagon, impotencija, azoospermija, kod žena - amenoreja, neplodnost.
Oštećenje zglobova očituje se upornom artralgijom, najčešće su zahvaćeni metakarpofalangealni zglobovi, rjeđe zglobovi koljena, kukova i laktova. Ukočenost zglobova se postepeno razvija.
Ostale kliničke manifestacije NG uključuju izrazitu nemotiviranu slabost, umor, pospanost, bolove u trbuhu različitog intenziteta i lokalizacije, hiperpigmentaciju kože i sklonost različitim infekcijama (uključujući mikroorganizme koji rijetko utječu na zdrave ljude - Yersenia enterocolitica i Vibrio vulnificus).
Dijagnoza NG se postavlja na osnovu karakteristične kliničke i laboratorijske slike.Lako je posumnjati na dijagnozu hemokromatoze kod pacijenta s kombinacijom sljedećih simptoma: artralgija, bol u trbuhu, brončano-siva koža, prisustvo dijabetesa melitusa i hepatomegalije.
Krvni test: karakteristična je kombinacija visokog nivoa hemoglobina i niske koncentracije hemoglobina u eritrocitima (SIT). Razvoj anemije ili druge citopenije primjećuje se u kasnim fazama bolesti - kod bolesnika sa cirozom jetre ili je rezultat brojnih krvožilnih bolesti.
Proučavanje metabolizma gvožđa je potrebno za prepoznavanje laboratorijskih znakova preopterećenja željezom i uključuje određivanje nivoa željeza, feritina i transferrina u krvnom serumu, ukupnog kapaciteta vezivanja željeza u serumu (OGSS) i procijenjeni koeficijent zasićenosti željeza transferinom (NTZH). NG karakteriše porast nivoa željeza i feritina u serumu, smanjenje nivoa OGSS i transferrina. Važan laboratorijski znak hemokromatoze je porast koeficijenta STI kod muškaraca iznad 60%, kod žena - iznad 50%.
Desferal test omogućava vam da potvrdite prisustvo preopterećenja željezom: nakon intramuskularnog 0,5 g deferoksamina (desferal), dnevno izlučivanje željeza u urinu značajno prelazi normalnu razinu (0-5 mmol / dan).
NG tipa IV, laboratorijska slika može biti predstavljena dubokom hipohromnom anemijom, hiposiderinemijom i povišenim seritnim feritinom, što je u kombinaciji s jakim preopterećenjem željezom.
Provođenje molekularno-genetske analize omogućava vam potvrđivanje nasljedne prirode hemokromatoze i isključenje sekundarne prirode preopterećenja gvožđem. Dijagnoza NG se postavlja u prisutnosti homozigotnih mutacija gena HFE (C282Y ili H63D) ili kada se otkriju složeni heterozigoti (kombinacija heterozigotnih mutacija C282Y i H63D) u bolesnika koji imaju laboratorijske znakove preopterećenja željezom. Izolovane heterorozne mutacije C282Y i H63D nalaze se u populaciji zdravih ljudi s učestalošću od 10,6%, odnosno 23,4% slučajeva, prisutnost ovih mutacija nije osnova za dijagnozu NG.
CT pretraga trbušnih organa otkriva povećanu gustoću jetrenog tkiva zbog depozita gvožđa i omogućava sumnju na prisustvo hemokromatoze.
Sa MRI jetra pacijenta s hemokromatozom ima tamno sivu ili crnu boju. CT i MRI jetre potrebni su za isključenje dijagnoze hepatocelularnog karcinoma.
Biopsija jetre s polukvantitativnim ili kvantitativnim određivanjem sadržaja željeza omogućava vam određivanje stupnja razvoja fibroze i koncentracije željeza u tkivu jetre. Za dijagnozu hemohromatoze preporučuje se izračunavanje "hepatičnog željeznog indeksa" koji je jednak omjeru sadržaja željeza u jetrenom tkivu (u mikromol / g suve težine) i pacijentove dobi (u godinama). Indeks> 2,0 potvrđuje dijagnozu NG.
Nasljedna hemokromatoza mora se razlikovati sa sekundarnim sindromima preopterećenja gvožđem, koji se razvijaju kod pacijenata s nasljednom i stečenom hemolitičkom anemijom, nekim oblicima mijelodisplastičnog sindroma (vatrostalna sideroblastična anemija), porfirijom, kao i u bolesnika s alkoholnim oštećenjem jetre.
Cilj liječenja NG-om je uklanjanje viška željeza iz tijela i sprečavanje nepovratnog oštećenja unutrašnjih organa. Uobičajena metoda lečenja je iscjedak krvi. Početni kurs sastoji se od prokrvljevanja krvi u količini od 500 ml jednom nedeljno. Nakon snižavanja nivoa hemoglobina za 15-20 g / l, nivo MCV za 3-5 fl. i sadržaj seritnog feritina do 20-50 ng / ml, pređite na terapiju za održavanje - uklanjanje 500 ml krvi svaka 2-4 mjeseca kod muškaraca i svaka 3-6 mjeseci u žena. Tretman je doživotni.
U prisustvu anemije ili drugih kontraindikacija (na primjer, zatajenje srca), helatori željeza koriste se za prokrvljenost krvi. Deferoksamin veže višak gvožđa u tkivima i krvnom serumu te se izlučuje urinom i izmetom. Međutim, poluživot ovog lijeka je kratak - samo 10 minuta, što zahtijeva sporo davanje: intravenski u obliku 3-4 sata infuzije ili subkutano, po mogućnosti u obliku 12-satnih ili cjelodnevnih infuzija pomoću posebnih pumpi. Razvijeni su novi lijekovi za oralno davanje složenog oblika koji su u fazi kliničkog proučavanja ili primjene, od kojih je najefikasnija Deferasirox.
Učinkovitost liječenja određuje se dinamikom kliničkih i laboratorijskih podataka. Stanje bolesnika počinje se poboljšavati nakon kursa krvotoka: nestaju slabost, umor, pospanost, smanjuje se veličina jetre, tijek dijabetesa i kardiomiopatije može se poboljšati. Laboratorijska kontrola uključuje proučavanje hemograma, pokazatelja feritina, željeza i NTZH (1 put u 3 mjeseca), nivo izlučivanja željeza u mokraći.
U slučaju rane dijagnoze hipertenzije i pravodobnog terapijskog krvotoka, prognoza je povoljna: životni vijek pacijenata ne razlikuje se od životnog vijeka ljudi koji ne pate od hemokromatoze. U slučajevima kasne dijagnoze bolesti, uz cirozu jetre, kardiomiopatiju, dijabetes melitus, prognoza se određuje težinom ovih nepovratnih komplikacija. Glavni uzroci smrti pacijenata su: komplikacije dijabetesa, zatajenja srca, primarni karcinom jetre, zatajenje jetre, krvarenje iz varikoznih vena jednjaka i želuca, interkurencijske infekcije.
Opće informacije
Hemohromatoza (brončani dijabetes, pigmentna ciroza) genetski je uzrokovana kršenjem metabolizma željeza, što dovodi do taloženja pigmenata koji sadrže željezo u tkivima i organima i do nastanka zastoja u više organa. Bolest, popraćena karakterističnim kompleksom simptoma (pigmentacija kože, ciroza jetre i dijabetes melitus) opisana je 1871. godine, a 1889. godine nazvana je hemohromatozom zbog karakteristične boje kože i unutrašnjih organa. Učestalost nasljedne hemokromatoze u populaciji iznosi 1,5-3 slučaja na 1000 stanovnika. Muškarci pate od hemohromatoze 2-3 puta češće od žena. Prosječna starost razvoja patologije je 40-60 godina. Zbog polisistemske prirode lezije, u proučavanju hemokromatoze uključene su različite kliničke discipline: gastroenterologija, kardiologija, endokrinologija, reumatologija itd.
U etiološkom aspektu razlikuju se primarna (nasljedna) i sekundarna hemokromatoza. Primarna hemokromatoza povezana je sa oštećenjem enzimskih sistema što dovodi do taloženja željeza u unutrašnjim organima. Ovisno o genskom defektu i kliničkoj slici, razlikuju se 4 oblika nasljedne hemokromatoze:
- I - klasični autozomno recesivni, HFE-povezani tip (više od 95% slučajeva)
- II - maloljetni tip
- III - nasljedni HFE-asocirani tip (mutacije u receptoru transferrina, tip 2)
- IV - autosomno dominantni tip.
Sekundarna hemokromatoza (generalizirana hemosideroza) razvija se kao rezultat stečene insuficijencije enzimskih sustava koji sudjeluju u metabolizmu željeza i često je povezana s drugim bolestima, u vezi s kojima se razlikuju njegove sljedeće varijante: post-transfuzijska, prehrambena, metabolička, miješana i neonatalna.
U kliničkom toku hemokromatoza prolazi kroz 3 stadija: I - bez preopterećenja gvožđem, II - sa preopterećenjem gvožđem, ali bez kliničkih simptoma, III - s razvojem kliničkih manifestacija.

Uzroci hemohromatoze
Primarna nasljedna hemokromatoza je autosomno recesivni poremećaj prenošenja. Zasniva se na mutacijama HFE gena smještenog na kratkom kraku 6. hromozoma. Neispravnost HFE gena dovodi do poremećaja unosa gvožđa posredovanog transferinom ćelijama dvanaestopalačnog crijeva 12, što rezultira stvaranjem lažnog signala o nedostatku željeza u tijelu. S druge strane, to doprinosi povećanoj sintezi proteina koji veže gvožđe DCT-1 enterocitima i povećanoj apsorpciji gvožđa u crevima (uz normalan unos elemenata u tragovima iz hrane). U budućnosti dolazi do pretjeranog taloženja pigmenta hemosiderina koji sadrži željezo u mnogim unutrašnjim organima, umiranje njihovih funkcionalno aktivnih elemenata s razvojem sklerotičnih procesa. Pomoću hemokromatoze, u ljudskom tijelu se godišnje nakuplja 0,5-1,0 g željeza, a manifestacije bolesti očituju se kada je dostignuta ukupna razina željeza od 20 g (ponekad i 40-50 g ili više).
Sekundarna hemokromatoza nastaje kao rezultat prevelikog egzogenog unosa gvožđa u organizam. Ovo se stanje može javiti čestim ponovljenim transfuzijama krvi, nekontrolisanim unosom željeznih pripravaka, talasemijom, nekim vrstama anemije, porfirije kože, alkoholne ciroze jetre, hroničnim virusnim hepatitisom B i C, zloćudnim novotvorinama, nakon dijeta sa malo proteina.
Simptomi hemohromatoze
Klinička manifestacija nasljedne hemokromatoze javlja se u odrasloj dobi, kada ukupni sadržaj željeza u tijelu dostigne kritične vrijednosti (20-40 g). Ovisno o prevladavajućim sindromima razlikuju se hepatopatski (hemokromatoza jetre), kardiopatski (srčana hemokromatoza), endokrinološki oblici bolesti.
Bolest se razvija postepeno, u početnoj fazi prevladavaju nespecifične žalbe zbog povećanog umora, slabosti, gubitka težine, smanjenog libida. U ovoj fazi bolesnike može uznemiriti bol u desnom hipohondriju, suva koža, artralgija zbog hondrokalcinoze velikih zglobova. U proširenom stadiju hemokromatoze formira se klasični simptomski kompleks predstavljen pigmentacijom kože (bronzana koža), cirozom, dijabetes melitusom, kardiomiopatijom, hipogonadizmom.
Obično je najraniji znak hemokromatoze pojava specifične boje kože i sluznica, koja se izražava uglavnom na licu, vratu, gornjim udovima, u pazuhu i vanjskim genitalijama, te na ožiljcima na koži. Intenzitet pigmentacije ovisi o trajanju tijeka bolesti i varira od blijedo sive (dimne) do brončano-smeđe. Karakteristično je opadanje kose na glavi i trupu, konkavna (u obliku žlice) deformacija noktiju. Primjećuju se artropatije metakarpofalangealnih, ponekad i zglobova koljena, kukova i lakta s naknadnim razvojem njihove krutosti.
Gotovo kod svih pacijenata otkriva se povećanje jetre, splenomegalija, ciroza jetre. Disfunkcija gušterače izražena je razvojem dijabetes melitusa ovisnog o insulinu. Kao posljedica oštećenja hipofize tijekom hemokromatoze, seksualna funkcija pati: kod muškaraca se razvija atrofija testisa, impotencija, ginekomastija, kod žena - amenoreja i neplodnost. Srčana hemokromatoza karakterizira kardiomiopatija i njene komplikacije - aritmija, hronično zatajenje srca, infarkt miokarda.
U terminalnom stadijumu hemokromatoze razvija se portalna hipertenzija, ascites, kaheksija. Smrt pacijenata u pravilu nastaje kao posljedica krvarenja iz varikoznih vena jednjaka, zatajenja jetre, akutnog zatajenja srca, dijabetičke kome, aseptičnog peritonitisa, sepse. Hemohromatoza značajno povećava rizik za razvoj raka jetre (hepatocelularni karcinom).
Dijagnoza hemohromatoze
Ovisno o prevladavajućim simptomima, pacijenti sa hemokromatozom mogu potražiti pomoć od raznih specijalista: gastroenterologa, kardiologa, endokrinologa, ginekologa, urologa, reumatologa i dermatologa. U međuvremenu, dijagnoza bolesti je ista za različite kliničke varijante hemokromatoze. Nakon procjene kliničkih znakova, pacijentima se dodjeljuje skup laboratorijskih i instrumentalnih studija kako bi se potvrdila valjanost dijagnoze.
Laboratorijski kriteriji za hemokromatozu su značajno povećanje razine željeza, feritina i transferrina u krvnom serumu, povećanje izlučivanja željeza u urinu i smanjenje ukupne sposobnosti vezivanja željeza u krvnom serumu. Dijagnoza se potvrđuje punkcijskom biopsijom jetre ili kože u čijim se uzorcima otkriva taloženje hemosiderina. Nasljedna priroda hemokromatoze utvrđena je kao rezultat molekularno-genetske dijagnostike.
Da bi se procijenila težina oštećenja unutarnjih organa i prognoza bolesti, proučavaju se jetreni testovi, koncentracije glukoze u krvi i urinu, glikozilirani hemoglobin i dr. Laboratorijska dijagnoza hemokromatoze dopunjava se instrumentalnim studijama: zajednička radiografija, EKG, ehokardiografija, ultrazvuk trbušne šupljine, MRI jetre i dr.
Liječenje hemohromatoze
Glavni cilj terapije je uklanjanje viška željeza iz tijela i sprečavanje razvoja komplikacija. Pacijentima sa hemokromatozom propisana je dijeta koja ograničava hranu bogatu gvožđem (jabuke, meso, jetra, heljda, špinat i dr.), Lako probavljivi ugljikohidrati. Zabranjeno je uzimanje multivitamina, askorbinske kiseline, dijetetskih dodataka koji sadrže željezo, alkohol. Da uklonite višak željeza iz organizma, pribjegavaju se krvotoku pod kontrolom hemoglobina, hematokrita i feritina. U tu svrhu se mogu koristiti ekstrakorporalne metode hemokorekcije - plazmafereza, hemosorpcija, citafereza.
Patogenetska terapija lijekovima hemokromatoze temelji se na intramuskularnoj ili intravenskoj primjeni deferoksaminskih vezivnih iona Fe3 + pacijentu. Istovremeno se provodi simptomatsko liječenje ciroze jetre, zatajenja srca, dijabetes melitusa i hipogonadizma. Kod teške artropatije određuju se indikacije za artroplastiku (endoprotetika zahvaćenih zglobova). U bolesnika sa cirozom rješava se pitanje transplantacije jetre.
Predviđanje i prevencija hemohromatoze
Uprkos progresivnom toku bolesti, pravovremena terapija može produžiti život pacijenata sa hemokromatozom za nekoliko decenija. U nedostatku liječenja, prosječni životni vijek pacijenata nakon dijagnoze patologije ne prelazi 4-5 godina. Prisutnost komplikacija hemokromatoze (uglavnom ciroza jetre i kongestivno zatajenje srca) prognostički je nepovoljan znak.
Nasljednom hemokromatozom prevencija se svodi na porodični skrining, rano otkrivanje i liječenje bolesti. Racionalna prehrana, nadzor primjene i primjene preparata željeza, transfuzije krvi, odbijanje pijenja alkohola i praćenje bolesnika sa bolestima jetre i krvožilnog sustava omogućuju izbjegavanje razvoja sekundarne hemohromatoze.